
乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制得:
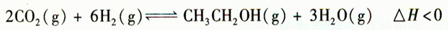
请回答:
(1)该反应的化学平衡常数表达式为 。
(2)当温度T1>T2时,化学平衡常数K1 K2(填“>”、“<”或“=”)。
(3)在恒温、恒容的密闭容器中,下列描述能说明上述反应已达化学平衡状态的是 (填字母序号)。
a.生成1molCH3CH2OH的同时生成3 mol H2O
b.容器中各组分浓度不随时间而变化
c.容器中混合气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(4)在工业生产中,可使H2的转化率和化学反应速率同时提高的措施有 (写出一条合理措施即可)。
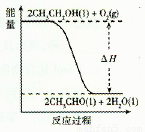
(5)工业上,常以乙醇为原料生产乙醛。根据下图所示信息,该反应是 反应(填“放热”或“吸热”),判断依据是__________________。
(6)乙醇可以作为燃料电池的燃料。某乙醇燃料电池以乙醇为燃料,使用酸性电解质,该电池负极反应的电极反应式为 。
(1)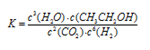 (2)< (3)b d (4)增大CO2浓度(或增大压强)
(2)< (3)b d (4)增大CO2浓度(或增大压强)
(5)放热 反应物总能量大于生成物总能量 (6)CH3CH2OH – 12 e- + 3H2O =2CO2 + 12H+
【解析】
试题分析:(1)根据化学平衡常数的定义,可知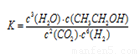
(2)当温度T1>T2时,由T1到T2,相当于是降低温度,降低温度,化学平衡向放热反应的方向进行,△H<0,即平衡右移,产物增多,反应物减少,因此,K1<K2。
(3)a.应符合“异方向、量相当”,生成1molCH3CH2OH的同时生成3 mol H2O,属于同一方向的描述,错误。
b.容器中各组分浓度不随时间而变化,属于化学平衡状态的定义,也是宏观判断标志,正确。
c.由于限定的条件是恒温、恒容的密闭容器中,反应前后质量守恒,因此,密度在反应的过程中未发生过变化,因此不能把容器中混合气体的密度不随时间而变化作为判断标志。 错误。
d.从化学方程式可以看出,该可逆反应是反应前后气体分子数减小的反应,当容器中容器中气体的分子总数不随时间而变化时,达到化学平衡,正确。
(4)根据可逆反应中,反应物的转化特点,当增加反应体系中另外一种物质CO2时,可使H2的转化率和化学反应速率同时提高,也可以增大压强。
(5)从函数图像可以看出,反应物自身具有的总能量高于生物自身具有的总能量,即E(反)>E(生)。
(6)CH3CH2OH中碳元素的化合价为-2价,在原电池的负极发生氧化反应,碳元素被氧化为CO2,化合价升高6价,CH3CH2OH中含有2个碳原子,1molCH3CH2OH被氧化,碳元素的化合价升高12价,即转移的电子数目为12e-,因此负极反应式为:CH3CH2OH – 12 e- + 3H2O =2CO2 + 12H+,正极反应式为: O2+4H++4e-=2H2O。
考点:考查化学平衡常数表达式的书写、化学平衡状态的判断标志、化学平衡移动、化学能与热能、原电池原理等知识。


科目:高中化学 来源: 题型:
| c(CH3OH)c3(H2O) |
| c2(CO2)c6(H2) |
| c(CH3OH)c3(H2O) |
| c2(CO2)c6(H2) |
| 温度/℃CO2转化率/% n(H2)/n(CO2) |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 (2012?湖南模拟)乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制得:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0
(2012?湖南模拟)乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制得:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g)△H<0| c(CH3CH2OH)?c3(H2O) |
| c2(CO2)?c6(H2) |
| c(CH3CH2OH)?c3(H2O) |
| c2(CO2)?c6(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| c3(H2O)?c(CH3OH) |
| c2(CO2)?c6(H2) |
| c3(H2O)?c(CH3OH) |
| c2(CO2)?c6(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制取:
乙醇是重要的化工原料和液体燃料,可以在一定条件下利用CO2与H2反应制取:| c(CH3CH2OH)?c3(H2O) |
| c2(CO2)?c6(H2) |
| c(CH3CH2OH)?c3(H2O) |
| c2(CO2)?c6(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
| c3(H2O)×c(CH3CH2OH) |
| c2(CO2)×c6(H2) |
| c3(H2O)×c(CH3CH2OH) |
| c2(CO2)×c6(H2) |
| 温度/℃CO2转化率/% n(H2)/n(CO2) |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com