
| A. | c(R2-)+c(OH-)=c(Na+)+c(H+) | B. | c(R2-)>c(Na+)>c(H+)=c(OH-) | ||
| C. | 2c(R2-)+c(HR-)=c(Na+) | D. | 混合后溶液的体积为2aL |
分析 常温下,混合溶液呈中性,则c(H+)=c(OH-),混合溶液中存在电荷守恒:2c(R2-)+c(OH-)+c(HR-)=c(Na+)+c(H+),再根据电荷守恒和弱电解质的性质进行判断.
解答 解:A.根据电荷守恒得:2c(R2-)+c(OH-)+c(HR-)=c(Na+)+c(H+),故A错误;
B.溶液呈中性c(H+)=c(OH-),溶液中存在电荷守恒2c(R2-)+c(OH-)+c(HR-)=c(Na+)+c(H+),所以c(Na+)>c(R2-),故B错误;
C.溶液呈中性c(H+)=c(OH-),溶液中存在电荷守恒2c(R2-)+c(OH-)+c(HR-)=c(Na+)+c(H+),所以2c(R2-)+c(HR-)=c(Na+),故C正确;
D.H2R+2NaOH═Na2R+2H2O,若H2R为强酸,根据H++OH-═H2O,两者反应显中性时,需要的H2R的体积为aL,总体积为2a L,但由于H2R是弱酸,浓度必大于10-3mol•L-1,所以两者反应呈中性时,消耗的H2R的体积小于aL,则混合后溶液的体积小于2a L,故D错误;
故选C.
点评 本题考查了酸碱混合溶液定性判断,题目难度中等,根据溶液的酸碱性结合电荷守恒解答,易错选项是D,注意先假设酸为强酸进行分析,再结合弱电解质浓度与其pH的关系分析解答.


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液褪色,而甲烷不能使酸性高锰酸钾溶液褪色 | |
| B. | 乙基对羟基的影响,使羟基的活性变弱,电离H+的能力不及H2O | |
| C. | 相等物质的量的甘油和乙醇分别与足量金属钠反应,甘油产生的H2多 | |
| D. | 苯酚中的羟基氢能与NaOH溶液反应,而醇羟基氢不能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多:2H++CO32-═H2O+CO2↑ | |
| B. | 氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2溶液至恰好为中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| D. | 碳酸氢钠溶液与过量的氢氧化钙溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 序号 | 1 | 2 | 3 | 4 | 5 | 6 |
| 导管及仪器 |  |  |  |  |  |  |
| 每个橡皮塞上都打了两个孔 | ||||||
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
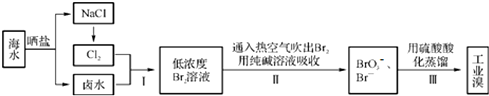
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com