
���� �ڽ������˳���У�λ����ǰ�Ľ����ܽ�λ�����Ľ�����������Һ���û���������װ���Ȼ�����Һ���ձ��У�����һ������Cu��Fe�Ļ�Ϸ�ĩ��������ͭ�������Ȼ�����Һ��Ӧ�������ԣ�FeCl3��CuCl2��FeCl2����ԭ��Fe��Cu��Fe��ʣ�࣬��Cuû�вμӷ�Ӧ����Һ�в�����Fe3+��Cu2+���Դ˽����⣮
��� �⣺�����ԣ�FeCl3��CuCl2��FeCl2����ԭ��Fe��Cu��
��1����Ӧ������ʣ�࣬����Fe+2FeCl3=3FeCl2��Fe+CuCl2=Cu+FeCl2��Fe3+��Cu2+�����ܴ��ڣ��ʴ�Ϊ��Fe3+��Cu2+��
��2����CuCl2��ʣ�࣬�����Ȼ�ͭ��������������������Fe�������п�����Fe3+��Fe2+��Cu��Fe2+���ʴ�Ϊ��Fe3+��Fe2+��Cu��Fe2+��
��3��FeCl3��CuCl2����ʣ�࣬��Fe��Cu����ȫ��Ӧ�����ܴ��ڣ�������һ������Fe2+���ʴ�Ϊ��Fe��Cu��Fe2+��
��4����FeCl3��ʣ�࣬����Fe+2FeCl3=3FeCl2��Cu+2FeCl3=CuCl2+2FeCl2��Fe��Cu�����ܴ��ڣ��ʴ�Ϊ��Fe��Cu��
��5���ɷ�ӦFe+2FeCl3=3FeCl2��Fe+CuCl2=Cu+FeCl2��������ǿ��˳��ΪFe3+��Cu2��Fe2+���ʴ�Ϊ��Fe3+��Cu2��Fe2+��
���� ���⿼��������ԭ��Ӧ�Լ����ĵ��ʻ���������ʣ���Ŀ�ѶȲ�����ؼ��ǰ������ʵ������ԡ���ԭ��ǿ���жϷ�Ӧ���Ⱥ�˳��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����������Ϊ���Ӿ��壮
����������Ϊ���Ӿ��壮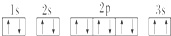 ����ͬѧ�����ĵ����Ų�ͼΥ��������ԭ����
����ͬѧ�����ĵ����Ų�ͼΥ��������ԭ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| �¶�/�� | 250 | 350 |
| K | 2.041 | x |
| c��CO��/mol•L-1 | c��H2��/mol•L-1 | c��CH3OH��/mol•L-1 | |
| 0min | 0.8mol•L-1 | 1.6mol•L-1 | 0 |
| 2min | 0.6mol•L-1 | y | 0.2mol•L-1 |
| 4min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
| 6min | 0.3mol•L-1 | 0.6mol•L-1 | 0.5mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢݢޢ� | B�� | �ۢܢ� | C�� | �ڢܢݢ� | D�� | �٢ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
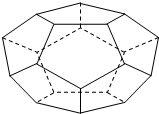 ��1����9��������NH2-����-NH2����Br-����OH-����-NO2����-OH����NO2��
��1����9��������NH2-����-NH2����Br-����OH-����-NO2����-OH����NO2���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20s�������n��H2����n��N2����n��NH3��=1��2��3 | |
| B�� | N2��ת����Ϊ30% | |
| C�� | 20s��H2��ƽ����Ӧ����Ϊ1.5mol•L-1•s-1 | |
| D�� | NH3���������Ϊ25% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com