
【题目】利用海水提取溴和镁的过程如下,下列说法不正确的是( )
A. 工业上常利用电解熔融MgCl2冶炼金属镁
B. 工业上可用NaBr溶液除去溴中含有的少量Cl2
C. 富集溴元素过程中,空气吹出法利用了溴易挥发的性质
D. 若提取1 mol Br2,至少需要标准状况下22.4 L的Cl2
【答案】D
【解析】依据流程分析,海水中加入氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤后在沉淀中加入盐酸溶解,得到氯化镁溶液,通过浓缩蒸发,冷却结晶得到氯化镁晶体,在氯化氢气流中加热失水得到无水氯化镁,电解熔融氯化镁得到金属镁;海水浓缩晒盐得到卤水中通入氧化剂氯气氧化溴离子得到溴单质,2Br-+C12=Br2+2Cl-,吹入热的空气用二氧化硫吸收富集溴SO2+Br2+2H2O=4H++2Br-+SO42-,通入氯气发生氧化还原反应生成单质溴。A.从MgCl2溶液中得到MgCl2固体,电解熔融氯化镁得到金属镁和氯气,反应的化学方程式为:MgCl2(熔融)![]() Mg+Cl2↑,故A正确;B.工业溴中含少量Cl2,用溴化钠溶液除去,反应的化学方程式为:Cl2+NaBr=+NaCl+Br2,溴被除去,故B正确;C.海水提取溴一般用氯气置换溴离子转化为溴单质,用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的,故C正确;D.若提取1 mol Br2,依据2Br-+Cl2=Br2+2Cl-,提取粗溴消耗氯气物质的量为:1mol,得到纯溴需氯气物质的量为:1mol,所以在标准状况下体积为V=nVm=2mol×224.4L/mol=44.8 L,故D错误;故选D。
Mg+Cl2↑,故A正确;B.工业溴中含少量Cl2,用溴化钠溶液除去,反应的化学方程式为:Cl2+NaBr=+NaCl+Br2,溴被除去,故B正确;C.海水提取溴一般用氯气置换溴离子转化为溴单质,用空气和水蒸气吹出单质溴,再用SO2将其还原吸收转化为HBr,达到富集的目的,故C正确;D.若提取1 mol Br2,依据2Br-+Cl2=Br2+2Cl-,提取粗溴消耗氯气物质的量为:1mol,得到纯溴需氯气物质的量为:1mol,所以在标准状况下体积为V=nVm=2mol×224.4L/mol=44.8 L,故D错误;故选D。


科目:高中化学 来源: 题型:
【题目】下列应用与盐类的水解无关的是( )
A. 明矾净水B. NaCl可用作防腐剂和调味剂
C. 热的纯碱溶液可去除油污D. FeCl3饱和溶液滴入沸水中制备Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以石油化工的一种产品A(乙烯)为主要原料合成一种具有果香味的物质E的生产流程如下:
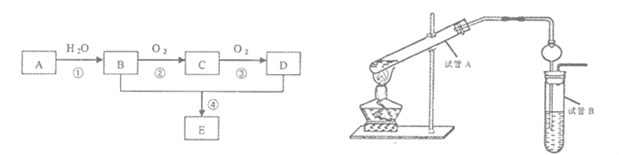
(1)写出步骤①的化学方程式_______________反应类型__________;
步骤②的化学方程式______________反应类型__________;
(2)某同学欲用上图装置制备物质E,回答以下问题:
①试管A发生反应的化学方程式_______________________;
②试管B中的试剂是______________________;分离出乙酸乙酯的实验操作是______________(填操作名称),用到的主要玻璃仪器为____________________;
③插入右边试管的导管接有一个球状物,其作用为_______________________。
(3)为了制备重要的有机原料——氯乙烷(CH3—CH2Cl),下面是两位同学设计的方案。
甲同学:选乙烷和适量氯气在光照条件下制备,原理是:
CH3—CH3+Cl2 ![]() CH3—CH2Cl+HCl
CH3—CH2Cl+HCl
乙同学:选乙烯和适量氯化氢在一定条件下制备,原理是:
CH2=CH2+HCl→CH3—CH2Cl
你认为上述两位同学的方案中,合理的是____,简述你的理由:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:

(1)a仪器的名称为_______;A装置中反应的化学方程式为_______。
(2)试剂b为_______;C装置的作用为_______。
(3)所用d导管较粗的原因是_______;E装置的作用为_______。
(4)F装置的作用为_______。
(5)若上图中的D、E装置改为下面装置,D装置中的现象为_______;用离子方程式表示E中的现象变化_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH-△H>0,下列叙述正确的是( )
A. 向平衡体系中加入水,平衡正向移动,c (H+)增大
B. 将水加热,Kw增大,pH不变
C. 向水中加入少量硫酸氢钠固体, 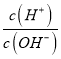 增大
增大
D. 向水中加入少量NaOH固体,平衡正向移动,c(H+)降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物阿司匹林可由水杨酸制得,它们的结构如图所示。有关说法正确的是( )
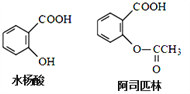
A. 1 mol阿司匹林最多可消耗3 molH2
B. 水杨酸分子中所有原子不可能共面
C. 水杨酸可以发生取代、加成、氧化、加聚反应
D. 1 mol阿司匹林最多可消耗2 molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列两个热化学方程式:
H2(g) + 1/2 O2(g) ![]() H2O(l) △H=-300KJ·mol-1
H2O(l) △H=-300KJ·mol-1
C3H8(g) + 5O2(g) ![]() 3CO2(g) + 4H2O(l) △H =-2000.0 KJ·mol-1
3CO2(g) + 4H2O(l) △H =-2000.0 KJ·mol-1
实验测得氢气的丙烷的混合气体共5mol,完全燃烧时放热5000KJ,则混合气体中氢气和丙烷的体积比约为( )
A. 7:10 B. 3:1 C. 10:7 D. 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、D、E、G、J在周期表中的位置如下: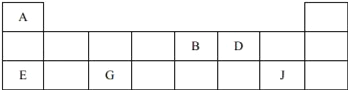
(1)根据上表回答问题:
①D在周期表中的位置是__.
②A、B、E、G的原子半径由大到小的顺序是__(填元素符号).
③B、D的气态氢化物的稳定性关系为__(填化学式).
④34Se与D同主族,其非金属性比D__(填“强”或“弱”),从原子结构的角度解释其原因为__.
⑤E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为ⅰ.H++OH﹣=H2O、ⅱ._________、ⅲ.________.
(2)如图所示转化关系中的各物质由以上六种元素的一种或多种组成,其中甲、乙、丙、丁为两种元素组成的化合物,甲、丙的分子属于10电子微粒,丙为常见溶剂.(图中部分产物已略)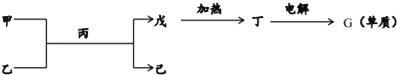
①物质己中含有的化学键的类型为__.
②用电子式表示丙分子的形成过程为__.
③由丁电解制得G单质的化学反应方程式为__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷雨天闪电时空气中有臭氧(O3)生成,下列说法中不正确的是( )
A.O2和O3互为同素异形体
B.O3是由3个氧原子构成的化合物
C.O2和O3相互转化属于化学变化
D.O3的摩尔质量为48g.mol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com