
| A. |  向AgNO3和CuCl2的混合溶液中缓慢通入氨水溶液 | |
| B. |  向NaOH和Ca(OH)2的混合溶液中通入CO2 | |
| C. | 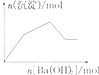 KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 | |
| D. | 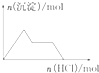 NaAlO2溶液中逐滴加入盐酸 |
分析 A.氨水过量时,氢氧化铜沉淀会溶解,图象与实际反应不相符;
B.首先生成碳酸钙白色沉淀,然后生成碳酸钠;继续通入CO2,碳酸钠和CO2反应生成碳酸氢钠,最后碳酸钙完全溶解生成碳酸氢钙;
C.铝离子和硫酸根分别和氢氧根和钡离子反应生成氢氧化铝和硫酸钡沉淀,然后形成的氢氧化铝被过量的氢氧根逐渐溶解,直到只剩余硫酸钡沉淀为止;
D.NaAlO2溶液中滴入盐酸溶液,先发生反应AlO2-+H++H2O═Al(OH)3↓生成沉淀,后发生反应Al(OH)3+3H+═Al3++3H2O,沉淀溶解至最后消失,结合前后两部分消耗盐酸溶液的体积判断.
解答 解:A.AgNO3和CuCl2的混合溶液中生成氯化银沉淀,然后缓慢通入氨水溶液中首先生成氢氧化铜沉淀,当氨水过量时生成的氢氧化铜溶解,所以图象曲线变化与实际反应不相符,故A错误;
B.向NaOH和Ca(OH)2的混合溶液中通入CO2,首先生成碳酸钙白色沉淀,然后生成碳酸钠;继续通入CO2,碳酸钠和CO2反应生成碳酸氢钠,最后碳酸钙溶解生成碳酸氢钙,图象与实际反应相符,故B正确;
C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液,开始阶段,铝离子和硫酸根分别和氢氧根和钡离子反应生成氢氧化铝和硫酸钡沉淀,然后形成的氢氧化铝被过量的氢氧根逐渐溶解,直到只剩余硫酸钡沉淀为止,大致反应图象为: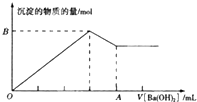 ,题中图象与实际反应不相符,故C错误;
,题中图象与实际反应不相符,故C错误;
D.NaAlO2溶液中滴入盐酸溶液,先发生AlO2-+H++H2O═Al(OH)3↓生成沉淀,后发生Al(OH)3+3H+═Al3++3H2O沉淀溶解至最后消失,反应图象为: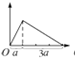 ,故D错误;
,故D错误;
故选B.
点评 本题考查离子反应的计算与图象判断,为高考的常见题型,属于中等难度的试题,解答关键是明确反应的原理,然后逐一分析,试题综合性强,旨在培养学生灵活运用基础知识解决实际问题的能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
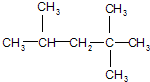 它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简
它是汽油燃烧品质抗震性能的参照物,用系统命名法对A进行命名,其名称为:2,2,4-三甲基戊烷;若A是由烯烃和H2通过加成反应得到,则该烯烃的结构简 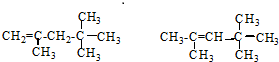 .
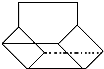
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | A | B | C | D |
| 性质 结构 信息 | 基态原子核外有两个电子层,最外层有3个未成对的电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中有一种是冶金工业常用的还原剂 |
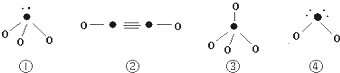
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com