
【题目】下列方程式正确的是( )
A.小苏打与盐酸反应的离子方程式:CO32+H+=CO2↑+H2O
B.乙烯与氯化氢加成的化学方程式:CH2=CH2+HCl![]() CH3=CH2Cl
CH3=CH2Cl
C.碳酸钾在水中的电离方程式:K2CO3![]() 2K++CO32
2K++CO32
D.醋酸钠水解的离子方程式:CH3COO+H2O![]() CH3COOH+OH
CH3COOH+OH
科目:高中化学 来源: 题型:
【题目】太阳能光电池由于具有充电快、寿命长等特点,适于很多特殊环境和场合,现已得到广泛应用。氮化稼(GaN)光电池的结构如图所示。下列说法中正确的是( )

A. 该装置系统中只存在两种能量转化
B. Cu电极上的电极反应为:CO2+8e-+8H+=CH4+2H2O
C. 离子交换膜为质子交换膜,H+从右池移向左池
D. 常温下,当装置中有lmolCH4生成时,GaN电极有44.8LO2生成(不考虑O2的溶解性〕
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示( )
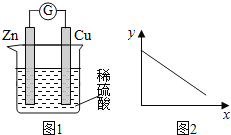
A. 铜棒的质量 B. c(Zn2+) C. c(H+) D. c(SO42-) -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷胺是最早用于抑制流感病毒的抗疾病毒药,其合成路线如图所示。下列说法不正确的是( )
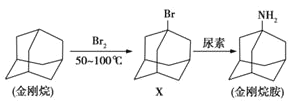
A. 金刚烷的分子式是C10H16B. X的一种同分异构体是芳香族化合物
C. 上述反应都属于取代反应D. 金刚烷的一溴代物有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池的反应方程式为 2MnO2+Zn+2H2O===2MnOOH+Zn(OH)2,其构造如图所示。有关说法不正确的是( )

A.负极反应式:Zn+2OH--2e-===Zn(OH)2
B.放电时正极MnO2得到电子,发生氧化反应
C.该电池使用一段时间后,电解液pH增大
D.放电时,锌粉失去的电子,从负极通过外电路流向正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期元素,若W原子的最外层电子数是其内层电子的![]() ,如图所示,下列说法不正确的是
,如图所示,下列说法不正确的是
X | Y | |
Z | W |
A.X元素的氢化物分子间可以形成氢键
B.Y元素的两种同素异形体常温下都是气体
C.阴离子半径从大到小的顺序为X>Y>Z>W
D.最高价氧化物对应的水化物的酸性:W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.66g镁铝合金加入到800mL稀硝酸中,恰好完全反应(假设反应中还原产物只有NO),向所得溶液中加入足量的3mol·L-1NaOH溶液,测得生成沉淀的质量与原合金的质量相等,则下列有关叙述不正确的是
A. 原稀硝酸的浓度为2.6mol·L-1 B. 生成NO的体积为11.648L(标准状况)
C. 反应过程中共消耗1.56molNaOH D. 合金中Al的质量分数约为58.6%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )
2SO3(g)(正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )
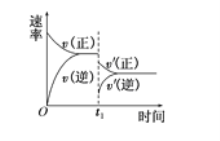
A. 催化剂失效 B. 减小生成物的浓度
C. 降低体系温度 D. 增大容器的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH溶液可用于多种气体的处理.
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3.
①Na2CO3俗称纯碱,因CO32﹣水解而使其水溶液呈碱性,可用于除油污,写出CO32﹣水解的离子方程式_______________________。
②泡沫灭火器中通常装有NaHCO3溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式_______________________。
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmolL﹣1CH3COONa溶液,则两份溶液中
c(NO3﹣)、c(NO2﹣)和c(CH3COO﹣)由大到小的顺序为_____(已知HNO2的电离常数Ka=7.1×10﹣4molL﹣1,CH3COOH的电离常数Ka=1.7×10﹣5molL﹣1)。可使溶液A和溶液B的 pH相等的方法是___。
A 向溶液A中加适量NaOH B 向溶液A中加适量水
C 向溶液B中加适量NaOH D 向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过裎中,溶液中H2SO3、HSO3﹣、SO32﹣三者所占物质的量分数(a)随pH变化的关系如图所示:

①图中pH=7时,溶液中离子浓度关系正确的是______。
A.c(Na+)>2c(SO32-)>c(HSO3-)
B.c(Na+)=c(SO32﹣) +c(HSO3﹣)+c(H2SO3)
C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO3﹣)
D.c(Na+)>c(HSO3﹣)>c(SO32﹣)> c(H+)=c(OH﹣)
②利用如图中数据,求H2SO3![]() H++ HSO3﹣的平衡常数的数值_____(保留两位小数)。
H++ HSO3﹣的平衡常数的数值_____(保留两位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com