
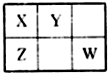
 X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若X原子的最外层电子数比其次外层电子数多3个,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中的位置如图所示.若X原子的最外层电子数比其次外层电子数多3个,下列说法正确的是( )| A、Y位于第二周期第ⅣA族 |
| B、非金属性:Y>Z>X |
| C、原子半径:Z>Y>X |
| D、X、W的氢化物相遇会产生白烟 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、①② | B、①②③ |
| C、①②④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 )与正丁醇发生酯化反应制得,下列有关说法不正确的是( )
)与正丁醇发生酯化反应制得,下列有关说法不正确的是( )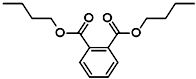
| A、邻苯二甲酸二丁酯(DBP)分子式为:C16H22O4 |
| B、邻苯二甲酸二丁酯(DBP)苯环上的一氯代物有2种 |
| C、邻苯二甲酸二丁酯(DBP)属于苯的同系物 |
| D、丁醇有4种不同结构,正丁醇是其中的一种,分子式为C4H10O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④⑤ | B、①②④⑤ |
| C、①②③④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、ab | B、bc | C、ac | D、ad |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、c(HCO
| ||||||
B、室温下,由水电离出的c(H+)=1×10-12 mol?L-1的溶液中:Fe2+、ClO-、Na+、SO
| ||||||
C、无色透明溶液中:SO
| ||||||
D、使红色石蕊试纸变蓝的溶液中:SO
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 单质 | 氧化物 | 酸 | 碱 | 盐 | |
| A | O3 | 水 | 硫酸 | 纯碱 | 胆矾 |
| B | 黄铜 | NO2 | 盐酸 | 石灰水 | FeSO4 |
| C | 碘酒 | 一氧化碳 | 磷酸 | NH3?H2O | 食盐 |
| D | H2 | Fe3O4 | HNO3 | 烧碱 | 小苏打 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com