
- 3 |
- 3 |
| A、元素R位于周期表中第VA族 | ||
B、RO
| ||
| C、R-离子的最外层电子数为8 | ||
D、若1molRO
|


科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、放电时,NaTi2(PO4)3发生氧化反应 |
| B、放电时,钠离子向负极移动 |
| C、充电时,阳极反应式为:Zn-2e-=Zn2+ |
| D、充电时,每移动0.2mol电子,消耗0.1mol Na3Ti2(PO4)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某元素由化合态变成游离态,该元素一定被氧化 |
| B、卤素离子(X-)只有还原性而无氧化性 |
| C、失电子难的原子获得电子的能力一定强 |
| D、负一价卤素离子的还原性在同一族中从上至下逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠跟水反应2Na+2H2O═2Na++2OH-+H2↑ |
| B、氨气通入醋酸溶液NH3+H+═NH4+ |
| C、铜与稀硝酸反应Cu+2NO3-+2H+=Cu2++NO2↑+H2O |
| D、碳酸钙溶于盐酸Ca2++2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
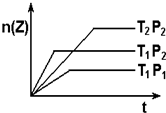 反应2X(g)+Y(g)?2Z△H<0 在不同温度和压强下,产物Z的物质的量与反应时间的关系如图所示.则下列叙述正确的是( )
反应2X(g)+Y(g)?2Z△H<0 在不同温度和压强下,产物Z的物质的量与反应时间的关系如图所示.则下列叙述正确的是( )| A、T1>T2,P1<P2 |
| B、T1>T2,P1>P2 |
| C、T1<T2,P1>P2 |
| D、T1<T2,P1<P2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,5.6g铁与足量的稀盐酸反应失去的电子数为0.3NA |
| B、11.2L CO2与8.5g NH3所含的分子数相等 |
| C、2g Na2O溶于水后,所得溶液中O2-个数为0.1NA |
| D、100mL 1mol?L-1 Na2SO4溶液中含Na+个数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯制溴乙烷:CH2CH2+Br2→CH2BrCH2Br | |||
B、乙醇催化氧化:2CH3CH2OH+O2
| |||
C、苯与氢气加成: | |||
| D、从海带中提取碘:H2O2+2I-+2H+=I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
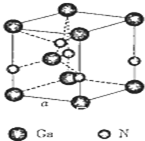 以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点.回答下列问题:
以氮化镓(GaN)为代表的第三代半导体材料目前已成为全球半导体研究的前沿和热点.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
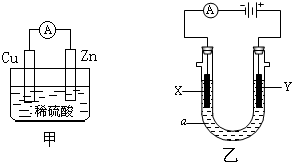 某化学兴趣小组的同学用如图装置研究电化学的问题.
某化学兴趣小组的同学用如图装置研究电化学的问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com