
| A、N2 |
| B、N2O |
| C、NO |
| D、NO2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计的水银球放置于蒸馏烧瓶的支管出口稍下处 |
| C、用容量瓶配制溶液时,加水超过了刻度线,没有采取补救措施,重新配制 |
| D、将5.85gNaCl溶于100mL水中,即配成1.0 mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7.8g Na2S和Na2O2的混合物中含有的离子总数为0.3NA |
| B、将1mol KClO3和SO3的混合物溶于水,溶液中自由移动的离子数目为3NA |
| C、标准状况下,22.4L氯气与足量的铁反应,转移电子数为0.2 NA |
| D、常温常压下,将0.1mol氯气通入水中发生化学反应,转移电子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它的原子核外有三种形状不同的电子云 |
| B、它的原子核外电子共有16种不同的运动状态 |
| C、它可与H2反应生成的化合物为非极性分子 |
D、核外电子轨道表示式为: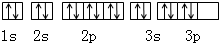 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com