
(8分)"比较"是化学研究物质性质的基本方法之一,请运用比较法解答下列问题.已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧 化物反应。
化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2,Na2O2+CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式。
(2)当1molSO3参加反应时,转移电子的物质的量为 mol。
(3)通过比较可知:在氧化物中,当非金属元素处于  价时,其氧化物与过氧化钠反应就有O2生成。
价时,其氧化物与过氧化钠反应就有O2生成。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
查看答案和解析>>
科目:高中化学 来源:2012届河南省焦作市高三第一次质量检测理综化学部分(带解析) 题型:填空题
(15分) 下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
| a | | | |||||||||||||||
| b | | | | c | d | e | f | | |||||||||
| g | h | i | j | | k | l | m | ||||||||||
| n | | | | | | | o | | | | | | | | | | |


查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)已知KMnO4和H2C2O4(草酸)在酸性溶液中会发生如下反应:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
 甲、乙两个实验小组欲探究影响化学反应速率的因素,设计
甲、乙两个实验小组欲探究影响化学反应速率的因素,设计
实验方案如下(实验中所用KMnO4溶液均已酸化):
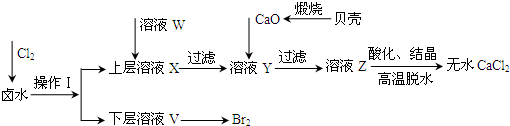
(1)甲组:通过测定单位时间内生成CO2气体体积的量来比
较化学反应速率,实验装置如图,实验时分液漏斗中A溶
液一次性加入,A、B的成分见下表:
| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1 mol·L-1H2C2O4溶液 | 4mL 0.01 mol·L-1KMnO4溶液 |
| ② | 2mL 0.2 mol·L-1 H2C2O4溶液 | 4mL 0.01 mol·L-1 KMnO4溶液 |
| ③ | 2mL 0.2 mol·L-1 H2C2O4溶液 | 4mL 0.01 mol·L-1 KMnO4溶液 少量MnSO4(催化剂) |
该实验探究的是 因素对化学反应速率的影响。在反应停止之前,相同时间内针筒中所得CO2的体积由大到小的顺序是 (填实验序号)。
(2)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率。
取两支试管各加入2 mL 0.1 mol·L-1H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol·L-1 KMnO4溶液。将四支试管分成两组(每组各有一支盛有H2C2O4溶液和KMnO4溶液),一组放入冷水中,另一组放入热水中,一段时间后,分别混合并振荡,记录溶液褪色所需时间。该实验试图探究
因素对化学反应速率的影响,但该组同学始终没有看到溶液完全褪色,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com