
【题目】下表是元素周期表的一部分,按要求完成各小题。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | ⑥ | ⑦ | ||||||
3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
4 | ② | ④ | ⑨ |
(1)元素①的元素符号:_______________
(2)元素⑧的单质电子式_______________
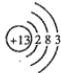
(3)元素⑤的原子结构示意图______________
(4)化学性质最不活泼的元素______(填元素符号,下同),非金属性最强的元素是________。金属性最强的单质_______。
(5)①③⑤三种元素的最高价氧化物水化物中,碱性最强的 _____(填化学式,下同)。①③⑤三种元素的原子半径由大到小的顺序为_____________。
(6)某元素的最高价氧物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,该元素的最高价氧化物和盐酸反应的化学方程式为 _____,与氢氧化钠溶液反应的化学方程式_____。
【答案】Na ![]()
 Ar F K NaOH r(Na)> r(Mg)> r(Al) Al2O3+6HCl=2AlCl3+3H2O Al2O3+2NaOH=2NaAlO2+H2O
Ar F K NaOH r(Na)> r(Mg)> r(Al) Al2O3+6HCl=2AlCl3+3H2O Al2O3+2NaOH=2NaAlO2+H2O
【解析】
根据元素在周期表中的位置知,①~11种元素分别是Na、K、Mg、Ca、Al、C、O、Cl、Br、Ar、F元素。
(1)根据元素在周期表中的位置知①的元素符号是Na,故答案为:Na;
(2)氯气分子中,2个氯原子通过共用一对电子,形成共价键,电子式为:![]() ,故答案为:
,故答案为:![]() ;
;
(3)Al的原子序数为13,原子核外有3个电子层,最外层电子数为3,则原子结构示意图为 ,故答案为:
,故答案为: ;
;
(4)这些元素中,Ar元素化学性质最不活泼,在这些元素中,非金属性最强的元素在周期表右上角,非金属性最强的元素是F,金属性最强的元素在周期表左下角,金属性最强的元素是K,故答案为:Ar;F;K;
(5)同一周期元素,从左到右,元素的金属性逐渐减弱,元素的金属性越强,其最高价氧化物是水化物碱性越强,①③⑤三种元素的最高价氧化物水化物中,碱性最强的是NaOH,同一周期元素,原子半径随着原子序数增大而减小,①③⑤三种元素的原子半径由大到小的顺序为r(Na)> r(Mg)> r(Al),故答案为:NaOH;r(Na)> r(Mg)> r(Al);
(6)元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐与水,为Al元素,该元素的最高价氧化物为Al2O3,它和盐酸反应的学方程式为:Al2O3+6HCl=2AlCl3+3H2O,与氢氧化钠溶液反应的化学方程式为Al2O3+2NaOH=2NaAlO2+H2O,故答案为:Al2O3+6HCl=2AlCl3+3H2O;Al2O3+2NaOH=2NaAlO2+H2O 。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组物质中,所含分子数相同的是
A.l0g H2和l0g O2B.9g H2O和0.5mol Br2
C.224mL H2(标准状况)和0.1mol N2D.5.6L N2(标准状况)和22g CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:

(1)如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂和C中相同,E中试剂所起的作用__,B装置除可检出某产物外,还可起到__作用。
(2)若进行上述实验时在F中得到10.0 g固体,则A中发生反应转移的电子数为__个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉煤气是炼铁厂排放的尾气,含有H2、N2、CO、CO2及O2,其中N2约为55%、CO约为25%、CO2约为15%、O2约为1.64%(均为体积分数)。某科研小组对尾气的应用展开研究:
(1)直接作燃料
已知:C(s)+O2(g)![]() CO2 (g) ΔH=-393.5kJ/mol
CO2 (g) ΔH=-393.5kJ/mol
2C(s)+O2(g)![]() 2CO (g) ΔH=-221kJ/mol
2CO (g) ΔH=-221kJ/mol
CO燃烧热的热化学方程式为__________。
(2)生产合成氨的原料
高炉煤气经过下列步骤可转化为合成氨的原料气:
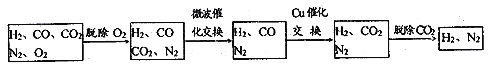
在脱氧过程中仅吸收了O2,交换过程中发生的反应如下,这两个反应均为吸热反应:
CO2+CH4![]() CO+H2(未配平) CO+H2O
CO+H2(未配平) CO+H2O![]() CO2+ H2
CO2+ H2
①气体通过微波催化交换炉需要较高温度,试根据该反应特征,解释采用较高温度的原因____________________________________________。
②通过铜催化交换炉后,所得气体中V(H2):V(N2)=__________。
(3)合成氨后的气体应用研究
①氨气可用于生产硝酸,该过程中会产生大气污染物NOx。为了研究对NOx的治理,该科研小组在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,发生如下反应:2NO(g)+Cl2(g)![]() 2ClNO(g) ΔH<0。10min时反应达平衡,测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=__________mol。设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为α2,则α1__________α2 (填“>”、“<”或“=”);平衡常数K__________(填增大”“减小 ”或“不变”)
2ClNO(g) ΔH<0。10min时反应达平衡,测得10min内v(ClNO)=7.5×10-3mol/(L·min),则平衡后n(Cl2)=__________mol。设此时NO的转化率为α1,若其它条件不变,上述反应在恒压条件下进行,平衡时NO的转化率为α2,则α1__________α2 (填“>”、“<”或“=”);平衡常数K__________(填增大”“减小 ”或“不变”)
②氨气还可用于制备NCl3,NCl3发生水解产物之一具有强氧化性,该水解产物能将稀盐酸中的NaClO2氧化成ClO2,该反应的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2004年是俄国化学家马尔柯夫尼柯夫(V.V.Markovnikov,1838—1904)逝世100周年。马尔柯夫尼柯夫因为提出碳碳双键的加成规则而闻名于世,该规则是指不对称的烯烃与HX或HCN加成时,氢总是加到含氢较多的双键碳原子上。
已知:CH3CH2CN![]() CH3CH3COOH
CH3CH3COOH
以下是某有机物F的合成路线,请填写下列空白。

(1)写出下列物质的结构简式A_______________,C_________________。
(2)B中官能团名称___________,反应②的反应类型是___________。
(3)写出③的化学方程式__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A—E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质。

(1)固体A的名称为____,单质B的常见用途有:_____(任写一条)。
(2)写出下列反应的化学方程式
①B→C__________
②A→D__________
(3)写出将氯气通入C溶液中的化学方程式_____,其溶液有漂白作用,漂白原理是______。(写反应方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池的说法不正确的是( )
A. 手机上用的锂离子电池属于二次电池
B. 铜锌原电池工作时,电子沿溶液从铜电极流向锌电极
C. 燃料电池的能量转换率超过80%
D. 锌锰干电池中,锌电极是负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 0.2 mol·L-1的NaCl液中含Na+的数目为0.2NA
B. 标准状况下,11.2L水中含有的水分子数目为0.5NA
C. S2和S8的混合物共6.4g,所含硫原子数一定为0.2NA
D. 将100mL0.1mol·L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶体粒子的数目为0.01NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量甘蔗渣,对甘蔗渣进行综合利用,可以提高经济效益,减少对环境的污染。如图所示为用甘蔗渣为原料制取各物质的转化过程图。
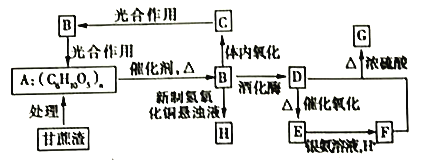
已知:①B在人体组织中发生缓慢氧化,放出热量,提供生命活动需要的能量。
②G是具有果香气味的液体,体积分数75%的D的水溶液常用于医疗消毒,并且可以代替汽油作汽车燃料。
③R—CHO![]() R—COOH
R—COOH
(1)A的化学名称为___________,B的分子式为___________。
(2)E的结构简式为___________,F分子中含有的官能团的名称为___________。
(3)D+F→G的化学方程式为___________,该反应的反应类型为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com