
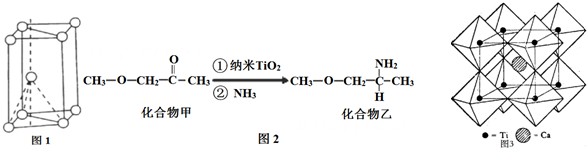
分析 (1)核外电子没有运动状态相同的电子;由金属钛晶胞结构可知,属于六方最密堆积;
(2)化合物甲与化合物乙均为分子晶体,但化合物乙分子间可形成氢键;化合物乙中C、N、O三种原子的杂化轨道形成均为sp3,同周期自左而右电负性增大;
(3)钛晶矿晶胞中钛离子与周围六个氧原子包围形成八面体,立方体晶胞共有12个边长,每条边长的中点是一个氧原子,共12个氧原子包围着中心的钙离子.
解答 解:(1)Ti原子核外电子数为22,核外共有22种运动状态不相同的电子;由金属钛晶胞结构可知,属于六方最密堆积;
故答案为:22;六方最密;
(2)化合物乙因分子间存在氢键,则化合物乙的沸点比化合物甲高,化合物乙中C、N、O三种原子的杂化轨道形成均为sp3,同周期自左而右电负性增大,故电负性:O>N>C,
故答案为:化合物乙分子间形成氢键;O>N>C;
(3)钛离子位于立方晶胞的角顶,被6个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被12个氧离子包围
故答案为:6.
点评 本题是对物质结构的考查,涉及核外电子排布、杂化轨道与空间构型、氢键、晶胞结构与计算等,需要显示具备一定的空间想象与数学计算能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L O2和O3的混合气中氧原子数为0.2NA | |
| B. | 标准状况下,22.4 L苯的分子数为NA | |
| C. | 46 g乙醇中含有的共价键总数为8 NA | |
| D. | 1 L 0.1 mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝热剂 | B. | 黑火药 | C. | 木炭 | D. | 丹药(硫化汞) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | A元素原子核外只有三个能级,且每个能级上含有相等的电子数 |
| B | 是空气中含量最丰富的元素 |
| C | 短周期元素中,C的金属性最强 |
| D | 基态原子第三能层上有7种运动状态不同的电子 |
| E | 一种核素的质量数为63,中子数为34 |
| F | 最外层电子数为次外层的3倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Cl只存在一种空间结构 | |
| B. | CH2Cl2只存在一种空间结构 | |
| C. | CHCl3只存在一种空间结构 | |
| D. | CH4的四个价键的键角和键长都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 闻名世界的中国陶瓷、酿酒、造纸技术都充分应用了化学工艺 | |
| B. | 植物油和矿物油都是碳氢化合物 | |
| C. | 光导纤维维、合成纤维和玻璃纤维都是新型无机非金属材料 | |
| D. | 蛋白质的水解和油脂的皂化都是由高分子生成小分子的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下可用铁制容器来盛装浓硫酸、说明常温下铁与浓硫酸不反应 | |
| B. | 同一元素的各种同位素的物理性质不同、化学性质相同 | |
| C. | 金属元素的原子只有还原性,离子只有氧化性 | |
| D. | 取碘水于试管中,加入汽油振荡后静置,其现象为下层呈紫红色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com