
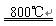
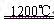 2Cu2O+2SO2
2Cu2O+2SO2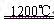 6Cu+SO2��
6Cu+SO2��A����Ӧ�� �����У�Cu2S��ֻ����ԭ�� �����У�Cu2S��ֻ����ԭ�� |
| B��1molCu2FeS2����1 mol Cu������������2.5 mol O2 |
| C��1molCu2S��O2��Ӧ����2 mol Cuת�Ƶĵ�����Ϊ4 mo1 |
| D����Ӧ���У���ת�Ƶĵ�����Ϊ16mol��CuFeS2��ͭԪ�صĻ��ϼ�Ϊ+2 |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����������ģ�ͣ� |
| B��CS2�ĵ���ʽ: S=C=S |
C��S2���Ľṹʾ��ͼ��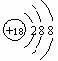 |
| D����ȩ�Ľṹ��ʽ��CH3COH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��100 mL H2��50 mL O2 | |
| B��100 mL NO��50 mL O2 | |
| C��100 mL HCl�� 50 mL NH3 | D��100 mL H2S�� 50 mL SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��6 | B��4 | C��3 | D��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ᡢ��������ƺ���ʯ�ҷֱ������ᡢ��κ������� |
| B��ͨ������£���������ӦA2 + 2B��= 2A��+ B2����ԭ�ԣ�B��> A�� |
| C������Ԫ��ԭ�������������Ķ��ٽ�Ԫ�ط�Ϊ����Ԫ�غͷǽ���Ԫ�� |
| D��̼��������ˮ�еĵ��뷽��ʽ��NaHCO3=Na++H++CO32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������������ʹ����е���������ʱ���������ĵ����⻯�ƶ� |
| B�������pHС�ڴ����pH |
| C��ϡ����ͬ�����������pH�� |
| D����Һ����������һ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A�������ӵ�ԭ�ӽṹʾ��ͼ��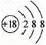 | B��������ӵ����ģ�ͣ�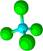 |
C����-�����ױ��Ľṹ��ʽ�� | D�������ǵ����ʽ��CH2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����״���£�11.2LSO3�����ķ�����Ϊ0.5 NA |
| B��1 mol Cl2�μ�������ԭ��Ӧ��ת�Ƶĵ�����Ŀһ����2 NA |
| C��������״̬�£�l mol NaHSO4��ȫ���������������ĿΪ2 NA |
| D��46 g����������������������������к��е�ԭ����Ϊ3 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��



| A��0.2 mol | B��0.4 mol | C��0.6 mol | D��0.8 mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com