
水的电离过程为H2O
 H++OH-,在不同温度下其平衡常数为:K(25℃)=1.0×10-14 mol2·L-2,K(35℃)=2.1×10-14 mol2·L-2。则下列叙述不正确的是( )
H++OH-,在不同温度下其平衡常数为:K(25℃)=1.0×10-14 mol2·L-2,K(35℃)=2.1×10-14 mol2·L-2。则下列叙述不正确的是( )
A.纯水的pH随着温度的升高而降低
B.在35℃时,[H+]>[OH-]
C.在25℃和35℃时,[H+]=[OH-]
D.水的电离是吸热的
科目:高中化学 来源: 题型:
据报道,我国拥有完全自主产权的氢氧燃料电池车已在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液。下列有关该电池的叙述不正确的是( )
A.正极反应式为:O2+2H2O+4e-===4OH-
B.工作一段时间后,电解液中KOH的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2===2H2O
D.该电池工作时每消耗1 mol O2,有2 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇广泛用作燃料电池的燃料,可用天然气来合成,已知:
①2CH4(g)+O2(g)===2CO(g)+4H2(g) ΔH=-71 kJ·mol-1
②CO(g)+2H2(g)===CH3OH(l) ΔH=-90.5 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
下列说法不能得出的结论是( )
A.反应②不需要加热就能进行
B.CO(g)+2H2(g)===CH3OH(g) ΔH>-90.5 kJ·mol-1
C.甲醇的燃烧热ΔH=-764 kJ·mol-1
D.若CO的燃烧热ΔH=-283.0 kJ·mol-1,则H2的燃烧热ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( ) 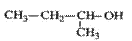
A. 的命名为:2-甲基-1-丙醇
B.软脂酸和油酸互为同系物
C.聚乙烯能使溴水褪色
D.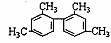 分子中至少有11个碳原子处于同一平面
分子中至少有11个碳原子处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天
然气(主要成分为CH4)与水进行高温重整制备合成气。
⑴ 已知:CH4、H2和CO的燃烧热(△H)分别为-890.3kJ/mol、-285.8kJ/mol和
-283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ。用1 m3(标准状况)的
甲烷与水蒸气在高温下反应制取合成气所需的热量为 (保留整数)。
⑵ 在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得
CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
|

 | 0 | 1 | 2 | 3 | 4 | ||||||
| CH4 | 0.2mol·L-1 | 0.13 mol·L-1 | 0.1 mol·L-1 | 0.1 mol·L-1 | 0.09 mol·L-1 | ||||||
| H2 | 0 mol·L-1 | 0.2 mol·L-1 | 0.3 mol·L-1 | 0.3 mol·L-1 | 0.33 mol·L-1 |
①计算该反应第一次达平衡时的平衡常数K 。
②3min时改变的反应条件是 (只填一种条件的改变即可)。
⑶ 已知温度、压强、投料比X对该反应的影响如图所示。

①图1中的两条曲线所示投料比的关系X1 X2(填“=”、“>”或“<”下同)。
②图2中两条曲线所示的压强比的关系:P1 P2。
⑷ 以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池:
①放电时,负极的电极反应式为 。
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下
的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列液体均处于25℃,有关叙述正确的是( )
A.某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐
B.pH=4.5的番茄汁中[H+]是pH=6.5的牛奶中[H+]的100倍
C.AgCl在同浓度的CaCl2和NaCl溶液中的溶解度相同
D.pH=5.6的CH3COOH与CH3COONa混合溶液中,[Na+]>[CH3COO-]
查看答案和解析>>
科目:高中化学 来源: 题型:
有一学生在实验室测某溶液的pH。实验时,他先用蒸馏水润湿pH试纸,然后用洁净干燥的玻璃棒蘸取试样进行检测。
(1)该学生的操作是__________(填“正确”或“错误”)的,其理由是
________________________________________________________________________。
(2)如不正确,请分析是否一定有误差
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)若用此法分别测定[H+]相等的盐酸和醋酸溶液的pH,误差较大的是__________,原因是________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(有机化学基础)蜂胶是一种天然抗癌药物,一个五六万只的蜂群一年只能产100多克蜂胶,所以蜂胶又被誉为“紫色黄金”。蜂胶的主要活性成分为咖啡酸苯乙酯,其分子结构如右图所示(短线表示化学键,如单键、双键等),在一定条件下能发生如下转化。
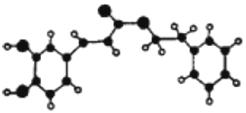
请回答下列问题:
(1)咖啡酸苯乙酯的分子式为 .C的结构简式为
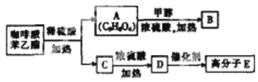
(2)①A中含氧官能团的名称为 、 。
②A可以发生的反应是 (填字毋)。
A、 加成反应B、酯化反应C、消去反应D、氧化反应
(3)高分子E的结构简式是 。
(4)C→D发生反应的反应类型是 。
(5)B的同分异构体有很多种,其中同时符合下列条件的同分异构体的结构简式为 。
a、苯环上只有两个取代基b.能发生银镜反应 c、能与氢氧化钠溶液反应
d、不能与氯化铁溶液发生显色反应 e、核磁共振氢谱图中有三组峰
查看答案和解析>>
科目:高中化学 来源: 题型:
在西安一座西汉古墓中出土了50多斤西汉时期的古酿,当开启酒坛封口时,散发出的香味把在场的品酒师都醉倒了,这些酒深藏地下历经两千年,不仅没有变质,反而变得香气更浓。这种香味是由哪种物质引起的( )
A.乙醇 B.乙酸
C.乙酸乙酯 D.乙醛
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com