
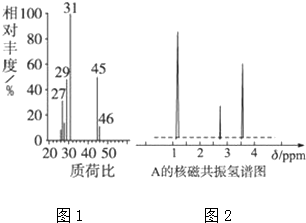
���� ��1��A��̼����������Ϊ52.16%�������������Ϊ13.14%������Ԫ����������=1-52.16%-13.14%=34.7%��Ȼ����ԭ�Ӹ���֮�ȣ�
��2�������Dzⶨ�л����������Է�������Ϊ46��������ʽ�жϷ���ʽΪC2H6O��
��3��A����Ϊ�Ҵ�������ѣ�
��4���л���A�����������ֲ�ͬ��ѧ��������ԭ�ӣ�ӦΪ�Ҵ���������ֻ��һ�ֲ�ͬ��ѧ��������ԭ�ӣ�
��� �⣺��1��A��̼����������Ϊ52.16%�������������Ϊ13.14%������Ԫ����������=1-52.16%-13.14%=34.7%��
���л��������N��C����N��H����N��O��=$\frac{52.16%}{12}$��$\frac{13.14%}{1}$��$\frac{34.7%}{16}$=2��6��1���ʴ�Ϊ��N��C����N��H����N��O��=2��6��1��
��2��ʵ��ʽΪC2H6O���л����������Է�������Ϊ46��ʵ��ʽ��Ϊ����ʽ��������ʵķ���ʽ��C2H6O��
�ʴ�Ϊ��46��C2H6O��
��3��A����Ϊ�Ҵ�������ѣ��ṹ��ʽΪCH3CH2OH��CH3OCH3���ʴ�Ϊ��CH3OCH3��CH3CH2OH��
��4���л���A�����������ֲ�ͬ��ѧ��������ԭ�ӣ�ӦΪ�Ҵ�����CH3CH2OH��������ֻ��һ�ֲ�ͬ��ѧ��������ԭ�ӣ��ʴ�Ϊ��CH3CH2OH��
���� ���⿼���л���ṹȷ������Ŀ�Ѷ��еȣ����غ�Ƕ��ж��л������ʽΪ������Ĺؼ���ע����������ͼ���˴Ź������ס�����������л���ṹȷ���е����ã�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� | �� | |
| 4 | �� | ⑪ | ⑫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2O��g��=H2O��l����H=-44kJ/mol�����Ըù����Ƿ��ȷ�Ӧ | |
| B�� | �������õ���Դ����ͨ����ѧ��Ӧ��õ� | |
| C�� | 2CO��g��+O2$\frac{\underline{\;��ȼ\;}}{\;}$2CO2��g����H��0����56gCO��32gO2�����е����������88g�����е������� | |
| D�� | ��Ҫ���ȵķ�Ӧһ�������ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ϩ���������Ϻͺϳ�����Ҫ�����л�ԭ�ϣ��ұ������ⷨ��Ŀǰ��������������ϩ����Ҫ�������仯ѧ����ʽΪ��
����ϩ���������Ϻͺϳ�����Ҫ�����л�ԭ�ϣ��ұ������ⷨ��Ŀǰ��������������ϩ����Ҫ�������仯ѧ����ʽΪ��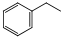 ��g��$?_{���£�T��}^{Fe_{2}O_{3}}$
��g��$?_{���£�T��}^{Fe_{2}O_{3}}$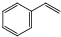 ��g��+H2��g����H=+120kJ•mol-1
��g��+H2��g����H=+120kJ•mol-1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�� | B�� | ���� | C�� | ���� | D�� | Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

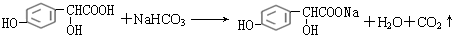 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
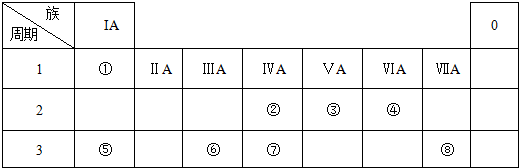
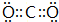 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | KOH��CaCl2�Ⱥ������Ӽ����ֺ��й��ۼ� | |
| B�� | PH3��ԭ�Ӿ�����8�����ȶ��ṹ | |
| C�� | �����ӵĽṹʾ��ͼ�� | |
| D�� | NH4Cl�ĵ���ʽ��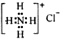 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com