
|
如图是在MgCl2、AlCl3混和溶液中,加入a或b时,沉淀物的量与加入的a或b的量的关系图,以下结论正确的是
①T之前加NaOH溶液,T之后加盐酸 ②T之前加盐酸,T之后加NaOH溶液 ③混和液c(AlCl3)∶c(MgCl2)=1∶1 ④图中所消耗的NaOH和HCl物质的量之比是3∶1 ⑤该盐酸与NaOH溶液的物质的量浓度相同 | |
| [ ] | |
A. |
①③④ |
B. |
①③⑤ |
C. |
②③④ |
D. |
②③⑤ |
科目:高中化学 来源: 题型:
 (2013?天河区一模)海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.
(2013?天河区一模)海水晒盐能够得到粗盐和卤水.卤水中含有MgCl2、KCl和MgSO4等物质,如图是它们的溶解度曲线.完成下列填空.查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 实验 编号 |
T/K | 反应 时间/h |
反应物的物质的量配比 n[CO(NH2)2]:n[MgCl2?6H2O] |
实验目的 |
| ① | 378 | 3 | 3:1 | (Ⅰ)实验①和③探究 反应物的物质的量配比对产率的影响 反应物的物质的量配比对产率的影响 删除此空 删除此空 ;(Ⅱ)实验②和④探究 温度对产率的影响 温度对产率的影响 ;(Ⅲ)实验②和 ③ ③ 探究反应时间对产率的影响. |
| ② | 378 | 4 | 4:1 | |
| ③ | 378 | 3 | ||
| ④ | 398 | 4 | 4:1 |

查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
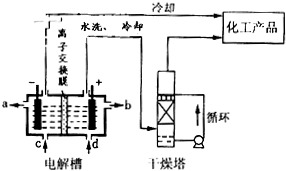
| ||
| ||
| △ |
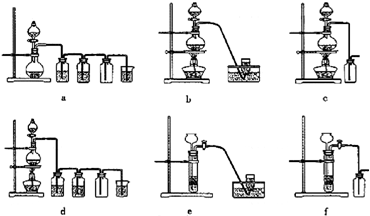
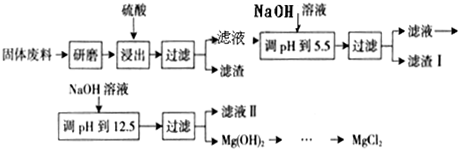
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |
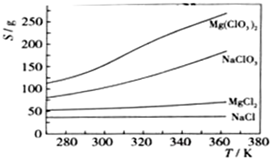
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com