
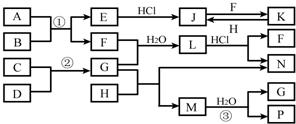
 ��ͼ�Dz��ֳ���Ԫ�صĵ��ʼ��仯�����ת����ϵͼ���йط�Ӧ�����������ɵIJ��ֲ�������ȥ����
��ͼ�Dz��ֳ���Ԫ�صĵ��ʼ��仯�����ת����ϵͼ���йط�Ӧ�����������ɵIJ��ֲ�������ȥ����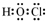 ��
������ EΪ����ɫ���壬��֪EΪFe2O3�������ᷴӦ����J��FeCl3��KΪdz��ɫ��Һ��ӦΪFeCl2���Ȼ������뵥��H��Ӧ�õ��Ȼ�������H��Cl2��F���Ȼ�����Ӧ�õ��Ȼ�������F���л�ԭ�ԣ�F���γ��������Ҫ����֮һ����FΪSO2����Ӧ���ǻ��������е���Ҫ��Ӧ����Ӧ�õ�E��F��Ӧ����������������Ӧ���������������������֪AΪFeS��N��һ�ֳ����ĵ��ʣ�������GΪ��ԭ��10���ӷ��ӣ�Ϊ����������G��NH3��G�������������Һ�з�Ӧ�õ�L��L�����ᷴӦ�õ�N�����������֪G���м��ԣ���ת����ϵ��֪��LΪ������炙���������泥���N��NH4Cl������C��D��Ӧ�õ�G��C��D�ֱ�Ϊ�����������е�һ�֣�������M������Ԫ����ɣ������ڹ���58�����ӣ��������백����Ӧ�õ���M��ˮ��Ӧ�õ�P��G����P��ˮ��Һ������Ư�����ã���M��NCl3��PΪHClO���ݴ˽��
��� �⣺EΪ����ɫ���壬��֪EΪFe2O3�������ᷴӦ����J��FeCl3��KΪdz��ɫ��Һ��ӦΪFeCl2���Ȼ������뵥��H��Ӧ�õ��Ȼ�������H��Cl2��F���Ȼ�����Ӧ�õ��Ȼ�������F���л�ԭ�ԣ�F���γ��������Ҫ����֮һ����FΪSO2����Ӧ���ǻ��������е���Ҫ��Ӧ����Ӧ�õ�E��F��Ӧ����������������Ӧ���������������������֪AΪFeS��N��һ�ֳ����ĵ��ʣ�������GΪ��ԭ��10���ӷ��ӣ�Ϊ����������G��NH3��G�������������Һ�з�Ӧ�õ�L��L�����ᷴӦ�õ�N�����������֪G���м��ԣ���ת����ϵ��֪��LΪ������炙���������泥���N��NH4Cl������C��D��Ӧ�õ�G��C��D�ֱ�Ϊ�����������е�һ�֣�������M������Ԫ����ɣ������ڹ���58�����ӣ��������백����Ӧ�õ���M��ˮ��Ӧ�õ�P ��G����P��ˮ��Һ������Ư�����ã���M��NCl3��PΪHClO��
��1����������ķ�����֪��M�Ļ�ѧʽΪNCl3��PΪHClO��P�ĵ���ʽΪ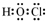 ��
��
�ʴ�Ϊ��NCl3��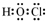 ��
��
��2��G��H��Ӧ�Ļ�ѧ����ʽΪ4NH3+3Cl2=NCl3+3NH4Cl��
�ʴ�Ϊ��4NH3+3Cl2=NCl3+3NH4Cl��
��3��KΪFeCl2�������������ӵķ����� ȡ������Ʒ���Թ��У���ˮ�ܽ⣬�μӸ��������Һ����Һ��ɫ��ȥ����˵����Fe2+����ȡ������Ʒ���Թ��У���ˮ�ܽ⣬�������軯����Һ�����μ���ˮ��Һ���Ѫ��ɫ����ȡ������Ʒ���Թ��У���ˮ�ܽ⣬����K3Fe��CN��6���������ɫ��������֤��ԭ��Һ����Fe2+��
�ʴ�Ϊ��ȡ������Ʒ���Թ��У���ˮ�ܽ⣬�μӸ��������Һ����Һ��ɫ��ȥ����˵����Fe2+����ȡ������Ʒ���Թ��У���ˮ�ܽ⣬�������軯����Һ�����μ���ˮ��Һ���Ѫ��ɫ����ȡ������Ʒ���Թ��У���ˮ�ܽ⣬����K3Fe��CN��6���������ɫ��������֤��ԭ��Һ����Fe2+��
��4����֪N2��H2��Ӧ����3.4gNH3��g����0.2mol��ʱ�ų�9.24kJ��������������2molNH3��g��ʱ�ų�92.4kJ�����������Ը÷�Ӧ���Ȼ�ѧ����Ϊ N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��
�ʴ�Ϊ��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��
��5��H��Cl2����ʵ�����У�����ˮ��Һ�м���CaCO3��ĩ����ַ�Ӧ����ˣ����Ƶ�Ũ�Ƚϴ��HClO��ˮ��Һ������Ϊ������ˮ��Һ�д���ƽ�⣺Cl2+H2O?H++Cl-+HClO�������CaCO3��ĩ��H+��Ӧ��ƽ�������ƶ���HClOŨ������
�ʴ�Ϊ��������ˮ��Һ�д���ƽ�⣺Cl2+H2O?H++Cl-+HClO�������CaCO3��ĩ��H+��Ӧ��ƽ�������ƶ���HClOŨ������
���� ���⿼�������ƶϣ��漰ת����ϵ�϶࣬�ۺϿ���ѧ����Ԫ�ػ�����֪ʶ���������������ʵ����ᡢ���ʵ�ʱ�ƶ�ͻ�ƿڣ�ע�������Ŀ�ṩ����Ϣ�����ƶϣ��ѶȽϴ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ɾ�ʢʳ�� | |
| B�� | ����Fe2O3�������ȷ�Ӧ����Ӧ������������� | |
| C�� | ������������θ����кͼ� | |
| D�� | ����������ˮ�����漰��ѧ�仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ʵ��������� | ʵ������ | ���� |
| ��ȡ���� | ����KSCN��Һ��Һ��죻 | ��Һ�д���Fe3+�� |
| ��ȡ���� | ��������KMnO4��Һ��ɫ��ȥ�� | ��Һ�д���Fe2+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҺΪdz��ɫ | |
| B�� | ��ҺΪ�ػ�ɫ | |
| C�� | �������軯����Һ�Ժ�ɫ | |
| D�� | �μ�NaOH��Һ��������ɫ�������ó��������ڿ����в���ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ�ı���̼������Һ��ͨ������CO2���� | |
| B�� | ���������Һ��ͨ���Ȼ������� | |
| C�� | ���Ȼ��ƺ�����Ļ����Һ��ͨ��SO2���� | |
| D�� | ����������Һ��ͨ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����һ�ַ�ɢϵ����ɢ���ǹ��� | |
| B�� | ����һ�ַ�ɢϵ����ɢ�������� | |
| C�� | �����ڽ����ɢϵ | |
| D�� | �������������в������ﳾ���Լ��������������γ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���и������ʣ��еľ��ж�������ţ�����д���пհף����ţ���
���и������ʣ��еľ��ж�������ţ�����д���пհף����ţ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ890.3 kJmor-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4��g��+202 ��g���TC02 ��g��+2H20��g����H=-890.3kJ mol-1 | |
| B�� | 500 V��30MPa�£���0.5molN2��1.5 molH2�����ܱյ������г�ַ�Ӧ���� NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ N2��g��+3H2 ��g��$?_{500�桢30Mp}^{����}$2NH3��g����H=-38.6 kJmol-1 | |
| C�� | ͬ��ͬѹ�£������ʵ�����H2��������C12�ڹ��պ͵�ȼ�����³�ַ�Ӧ����������������ͬ | |
| D�� | ��֪�к���Ϊ57.3 kJ/mol����ϡ����������������Һ��Ӧ���Ȼ�ѧ����ʽΪ 2H+��aq��+SO42-��aq��+Ba2+��aq��+20H-��aq��=BaS04 ��s��+2H20��l����H=-57.3kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com