
分析 (1)Al氧化生成氧化铝,氧化铝的熔点高;
(2)Al很快能被氧化为氧化铝;
(3)Al粉与氧气的接触面积大;
(4)氧化铝为致密的结构;增大反应的接触面积、反应温度均可实验铝燃烧实验;
(5)由上述实验可知,接触面积、反应温度影响燃烧实验.
解答 解:(1)在酒精灯上加热至熔化,轻轻晃动,观察到的现象是铝箔熔化,失去了光泽,熔化的铝并不滴落,好像有一层膜兜着,产生该现象的原因是构成铝表面氧化膜的Al2O3熔点高,包在铝的外面,使液态铝不滴落,
故答案为:铝箔熔化,失去了光泽,熔化的铝并不滴落,好像有一层膜兜着;成铝表面氧化膜的Al2O3熔点高,包在铝的外面,使液态铝不滴落;
(2)除去表面的保护膜,再用坩埚钳夹持在酒精灯上加热至熔化,结果观察到的现象与甲仍相同,其原因是除去氧化膜的铝在空气中又很快地生成一层新的Al2O3保护膜,故答案为:除去氧化膜的铝在空气中又很快地生成一层新的Al2O3保护膜;
(3)将铝粉撒到酒精灯火焰上(增大铝与空气的接触面积)可观察到铝在空气中燃烧,故答案为:将铝粉撒到酒精灯火焰上;
(4)铝在空气中能表现出良好的抗腐蚀性,是因铝易与空气中的氧气反应生成致密的氧化膜,阻止了内部的铝与空气接触,从而防止铝进一步被氧化;
铝燃烧的另一实验方案为将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到耀眼的白光(提高反应温度),
故答案为:铝易与空气中的氧气反应生成致密的氧化膜,阻止了内部的铝与空气接触,从而防止铝进一步被氧化;将铝箔卷曲,尖端夹一根火柴,将火柴引燃后,把火柴和铝箔一起伸入到盛有氧气的集气瓶中即可观察到耀眼的白光(提高反应温度);
(5)由上述实验可知,增大可燃物与空气的接触面积或提高反应的温度的方法可以观察到可燃物燃烧的现象,故答案为:增大可燃物与空气的接触面积或提高反应的温度.
点评 本题考查Al的化学性质,为高频考点,把握燃烧的条件及氧化铝的结构为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题

| A. | 用图1装置和方法测定一定时间内生成H2的反应速率 | |
| B. | 用图2装置和方法进行C02喷泉实验 | |
| C. | 用图3装装置和方法除去氯气中的氯化氢 | |
| D. | 用图4装置和方法比较Na2C03与NaHC03热稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.28 L | B. | 0.56 L | C. | 0.14 L | D. | 11.2 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水稀释2倍后,两溶液的pH均减小 | |
| B. | 使温度都升高20℃后,两溶液的pH均不变 | |
| C. | 加适量的醋酸钠晶体后,两溶液的pH均增大 | |
| D. | 加足量的锌充分反应后,醋酸和盐酸产生的氢气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
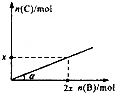 某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:A(s)+3B(g)?2C(g)+D(g);△H<0,在一定温度和压强下达到平衡.若平衡时C的物质的量与加入B的物质的量的变化关系如图所示.则下列说法中正确的是( )
某容积可变的密闭容器中盛有足量的A,通人气体B,发生反应:A(s)+3B(g)?2C(g)+D(g);△H<0,在一定温度和压强下达到平衡.若平衡时C的物质的量与加入B的物质的量的变化关系如图所示.则下列说法中正确的是( )| A. | 若保持压强不变,降低温度时,图中角度a将变小 | |
| B. | 若增大压强,缩小容器的体积,平衡向正反应方向移动 | |
| C. | 若保持压强不变,再通入B,则再次达到平衡时正、逆反应速率均增大 | |
| D. | 平衡时B、C的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O | B. | C+4HNO3(浓)═CO2↑+4NO2↑+2H2O | ||
| C. | 3Fe+8HNO3(稀)═3Fe(NO3)2+2NO↑+4H2O | D. | CuO+2HNO3(稀)═Cu(NO3)2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4是酸,因为H2SO4中含有氢元素 | |
| B. | 燃烧必须有氧气参与,因而没有氧气参与的反应一定没有燃烧现象 | |
| C. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 | |
| D. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.8g | B. | 15.3g | C. | 19.6g | D. | 30.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com