

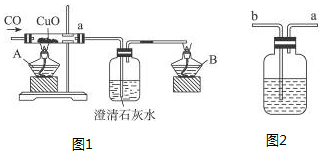
分析 (1)实验开始需要先用CO把装置中空气赶净,一氧化碳有毒污染空气需要尾气处理;
(2)硬质玻璃管中发生的反应为一氧化碳还原氧化铜生成铜和二氧化碳,结合反应物和生成物书写化学方程式;
(3)一氧化碳还原氧化铜后生成能使澄清石灰水变浑浊的气体;
(4)一氧化碳有毒,不能直接排放到空气中.
(5)从操作顺序分析判断,一氧化碳遇到空气点燃易发生爆炸;
(6)储气装置需要导气管短进长出;
(7)加热CuO前必须先通CO,此时即可观察CO是否能使澄清石灰水变浑浊.
解答 解:(1)实验开始需要先用CO把装置中空气赶净,一氧化碳有毒污染空气需要尾气处理,点燃酒精灯A、B的先后顺序为:先点燃酒精灯B,后点燃酒精灯A,
故答案为:B;A;
(2)硬质玻璃管中发生的反应为一氧化碳还原氧化铜生成铜和二氧化碳,化学方程式为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 ,
故答案为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2
(3)一氧化碳还原氧化铜生成铜和二氧化碳,二氧化碳能使澄清石灰水变浑浊,洗气瓶中的实验现象为:澄清石灰水变浑浊,
故答案为:澄清石灰水变浑浊;
(4)CO有毒,不能直接排放,用酒精灯点燃未反应的CO,可防止污染环境,酒精灯B的作用为点燃未反应的CO,防止污染环境,
故答案为:点燃未反应的CO,防止污染环境;
(5)将酒精灯合二为一,将尾气导管出口旋转到A的火焰上的做法不合理,因为CO点燃在前,CuO加热在后,不能同时进行,否则可能引起爆炸,
故答案为:不合理;因为CO点燃在前,CuO加热在后,不能同时进行,否则可能引起爆炸;
(6)用此装置贮存气体,就要把水排出,导气管需要短进长出,排水应从a进入气体,故答案为:a;
(7)在CO通人CuO前应先通入澄清石灰水的设计不必要,因为加热CuO前必须先通CO,此时即可观察CO是否能使澄清石灰水变浑浊.
故答案为:不必要.
点评 本题考查了实验基本操作、实验顺序的分析判断,解答本题要熟悉课本上相应的实验,能根据气体的性质和操作的目的进行相应的判断,从而得出正确答案,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
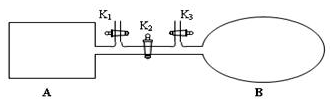 我国于2016年10月17日在酒泉卫星发射中心由“长征二号”FY11运载火箭发射“神舟十一号”载人飞船.“长征二号”FY11运载火箭使用的氧化剂是N2O4.如图,A是由导热材料制成的恒容密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,通过K1、K3分别向容器A、气囊B中充入1molNO2,发生反应:2NO2(g)?N2O4(g).反应起始时A、B的体积均为1L.
我国于2016年10月17日在酒泉卫星发射中心由“长征二号”FY11运载火箭发射“神舟十一号”载人飞船.“长征二号”FY11运载火箭使用的氧化剂是N2O4.如图,A是由导热材料制成的恒容密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2,通过K1、K3分别向容器A、气囊B中充入1molNO2,发生反应:2NO2(g)?N2O4(g).反应起始时A、B的体积均为1L.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
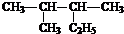 2,3-二甲基戊烷
2,3-二甲基戊烷查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,也称可吸入颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 浊液的分散质粒子直径大于l00nm,不能通过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2 | B. | N2 | C. | O2 | D. | CO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol NaHSO4晶体中含阴阳离子总数是0.3NA | |
| B. | 将0.1mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA | |
| C. | 1 mol Na2O2与足量H2O完全反应,转移电子数目为2NA | |
| D. | 在常温常压下,13.8g NO2与足量水充分反应,剩余气体的分子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com