
镁电池毒性低、污染小,电压高且平稳,它逐渐成为人们研究绿色电池的关注焦点。其中一种镁电池的反应原理为:xMg+ Mo3S4 MgxMo3S4,下列说法正确的是( )
MgxMo3S4,下列说法正确的是( )
A.放电时Mo3S4发生氧化反应
B.放电时,正极反应式为:Mo3S4 + 2xe- = Mo3S42x-
C.充电时,电路中通过2mol电子时,可消耗1mol Mg
D.充电时,Mg2+向负极移动
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:2015-2016学年河北省、永年二中高一下学期期中化学试卷(解析版) 题型:选择题
下列变化过程需要吸收能量的是( )
A.2H2+O2===2H2O B.CaO+H2O===Ca(OH)2
C.Cl+Cl―→Cl2 D.H2―→H+H
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中文科化学试卷(解析版) 题型:选择题
下列防止金属腐蚀的做法不可行的是
A.在某些工具的机械转动部位刷油漆以防锈
B.衣架和电线外面包上一层塑料层以防锈
C.在钢材制造的大型船舶上装上一定数量的锌块
D.自行车的钢圈和车铃上镀上一层铬,既耐腐蚀又美观耐磨
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高二下期中文科化学试卷(解析版) 题型:选择题
为使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于
A.无机物 B.非金属单质 C.盐类 D.有机物
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三第三次模拟理综化学试卷(解析版) 题型:填空题
某种锂离子电池的正极材料是将含有钴酸锂(LiCoO2)的正极粉均匀涂覆在铝箔上制成的,可以再生利用。某校研究小组尝试回收废旧正极材料中的钴。
(1)25℃时,用图1所示装置进行电解,有一定量的钴以Co2+的形式从正极粉中浸出,且两极均有气泡产生,一段时间后正极粉与铝箔剥离。
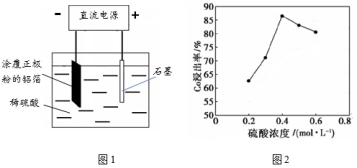
①阴极的电极反应式为:LiCoO2+4H++e-=Li++Co2++2H2O、 。
阳极的电极反应式为 。
②该研究小组发现硫酸浓度对钴的浸出率有较大影响,一定条件下,测得其变化曲线如图2所示。当c(H2SO4)>0.4mol/L时,钴的浸出率下降,其原因可能为
。
(2)电解完成后得到含Co2+的浸出液,且有少量正极粉沉积在电解槽底部。用以下步骤继续回收钴。

①写出“酸浸”过程中正极粉发生反应的化学方程式: 。该步骤一般在80℃以下进行,温度不能太高的原因是 。
②已知(NH4)2C2O4溶液呈弱酸性,下列关系中正确的是 (填字母序号)。
A.c(NH4+) > c(C2O42-) > c(H+) > c(OH-)
B.c(H+) + c(NH4+) = c(C2O42-) + c(OH-) + c(HC2O4-)
C.c(NH4+) + c(NH3·H2O) = 2[c(C2O42-) + c(HC2O4-) + c(H2C2O4 )]
(3)已知所用锂离子电池的正极材料为x g,其中LiCoO2 的质量分数为a%,则回收后得到CoC2O4·2H2O 的质量不高于 g。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:实验题
废弃物的综合利用既有利于节约资源,又有利于保护环境。工业上利用铅浮渣(主要成分是PbO、Pb还含有少量的Ag、CaO)可制备硫酸铅。制备流程图如下:

下表是25℃ 时某些盐的浓度积常数:
化学式 | CaSO4 | Ag2SO4 | PbSO4 |
Ksp | 4.9×10-5 | 1.2×10-5 | 1.6×10-8 |
(1)实验室用75%的硝酸来配制15%的硝酸溶液,不需用到的玻璃仪器有 (填标号)。
A.烧杯 B.量筒 C.容量瓶 D.锥形瓶 E.玻璃棒
(2)步骤I有NO产生,浸出液中含量最多的金属阳离子为 Pb2+,写出Pb参加反应的化学方程式 ,为防止Ag被溶解进入溶液,步骤I操作时应注意 。
(3)母液可循环利用于步骤I,其溶质主要是 (填一种物质化学式),若母液中残留的 SO42-过多,循环利用时可能出现的问题是 。
(4)粗PbSO4 产品含有的杂质是____________,需用 溶液多次洗涤,以得到纯净的PbSO4。
(5)铅蓄电池放电时正极的电极反应式为 。如果用铅蓄电池做电源电解饱和食盐水制取Cl2,已知某铅蓄电池中硫酸溶液的体积为0.80 L,电解前硫酸溶液浓度为4.50 mol·L-1,当制得4.48 LCl2时(在标准状况下),求理论上电解后电池中硫酸溶液的浓度为(假设电解前后硫酸溶液的体积不变)_________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三考前训练一理综化学试卷(解析版) 题型:选择题
乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,能在制备乙醛的同时获得电能,其总反应为:2CH2 =CH2 + O2 → 2CH3CHO。下列有关说法正确的是( )
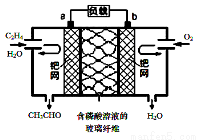
A.a电极发生还原反应
B.放电时,每转移2mol电子,理论上需要消耗28g乙烯
C.b极反应式为:O2+4e-+2H2O=4OH-
D.电子移动方向:电极a→磷酸溶液→电极b
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期中化学试卷(解析版) 题型:选择题
有下列有机反应类型:①消去反应②水解反应③加聚反应④加成反应⑤还原反应⑥氧化反应,以丙醛为原料制取1,2一丙二醇,所需进行的反应类型依次是( )
A.⑤①④② B.⑥④②① C.①③②⑤ D.⑤②④①
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一下期中化学试卷(解析版) 题型:选择题
将固体NH4Br置于密闭容器中,在某一温度下,发生下列反应:NH4Br(g) NH3(g) + HBr(g)
NH3(g) + HBr(g)
2HBr(g) H2(g) + Br2(g) ,两分钟后测得c(H2)为0.5mol/L-1,c(HBr)为4mol/L-1,若NH4Br的分解速率用v(NH3)表示,下列速率正确的是
H2(g) + Br2(g) ,两分钟后测得c(H2)为0.5mol/L-1,c(HBr)为4mol/L-1,若NH4Br的分解速率用v(NH3)表示,下列速率正确的是
A.0.5mol·L-1·min-1 B .2.5 mol·L-1·min-1
C.2 mol·L-1·min-1 D.5 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com