
氢气是清洁的能源,也是重要的化工原料,根据以下两种制氢方法,完成下列问题:
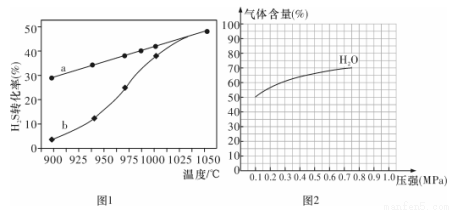
(1)方法一:H2S热分解法,反应式为:2H2S(g) 2H2(g) + S(g) △H,在恒容密闭容器中,测定H2S分解的转化率(H2S的起始浓度均为cmol/L),测定结果见图1,其中曲线a表示H2S的平衡转化率与温度关系,曲线b表示不同温度下反应经过相同时间未达到化学平衡时H2S的转化率。
2H2(g) + S(g) △H,在恒容密闭容器中,测定H2S分解的转化率(H2S的起始浓度均为cmol/L),测定结果见图1,其中曲线a表示H2S的平衡转化率与温度关系,曲线b表示不同温度下反应经过相同时间未达到化学平衡时H2S的转化率。
①△H ______0(填“>”“<”或“=”)。
②若985 ℃时,反应经t min达到平衡,此时H2S的转化率为40%,则tmin内反应速率v(H2)=________(用含c、t的代数式表示)。
③请说明随温度的升高,曲线b向曲线a接近的原因: _______________。
(2)方法二:以CaO为吸收体,将生物材质(以C计)与水蒸气反应制取H2。相关主要反应如下:
I.C(s)+H2O(g)==CO(g)+H2(g)△H=+131.6kJ/mol
II.CO(g)+H2O(g)==CO2(g)+H2(g)△H=-43kJ/mol
III.CaO(s)+CO2(g)==CaCO3(s)△H=-178.3kJ/mol
①计算反应C(s)+2H2O(g)+CaO(s)==CaCO3(s)+2H2(g)的△H =________(保留到小数点后面1位);若K1、K2、K3分别为反应I、II、III的平衡常数,该反应的平衡常数k=_________(用K1、K2、K3表示)。
② 对于可逆反应 C(s)+2H2O(g)+CaO(s) CaCO3(s) + 2H2(g),采取以下措施可以提高H2产率的是___________。(填字母编号)
CaCO3(s) + 2H2(g),采取以下措施可以提高H2产率的是___________。(填字母编号)
A.适当的降低体系的温度 B.压缩容器的体积
C.用特殊材料吸收氢气 D.增加CaO的量
③ 图2为反应I在一定温度下,平衡时各气体体积百分含量随压强变化的关系图。若反应达某一平衡状态时,测得c( H2O) = 2c(H2)= 2c(CO) = 2 mol/L,试根据H2O的体积百分含量变化曲线,补充完整 CO的变化曲线示意图。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年四川省高一上半期考试化学卷(解析版) 题型:选择题
氧化还原反应的实质是( )
A.氧元素的得失 B.化合价的升降
C.电子的得失或偏移 D.分子中原子的重新组合
查看答案和解析>>
科目:高中化学 来源:2017届西藏山南二中高三上11月月考化学试卷(解析版) 题型:选择题
下列有关阿伏加德罗常数为(NA)的说法错误的是( )
A.0.5NA个氯气分子的物质的量是0.5 mol
B.1 mol H2O含有的H2O分子数目为NA
C. 0.5 mol H 2O含有的原子数目
2O含有的原子数目 为NA
为NA
D. 32 g O2所含的氧原子数目为2NA
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次段考化学卷(解析版) 题型:选择题
该同学用如下装置进行实验,分析影响反应速率的因素:
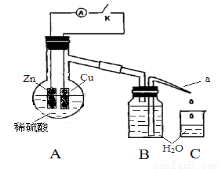
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示。下列说法不正确的是
实验Ⅰ(断开K)1分钟水滴数 | 34 | 59 | 86 | 117 | … | 102 |
实验Ⅱ(闭合K))1分钟水滴数 | 58 | 81 | 112 | 139 | … | 78 |
A.实验Ⅰ中化学能主要转化为热能
B.实验Ⅱ中化学能主要转化为电能
C.反应前期水滴数58>34、81>59,主要原因是实验Ⅱ中形成原电池加快反应速率
D.反应后期水滴数102>78,主要原因是实验Ⅰ溶液温度高于实验Ⅱ
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上第二次段考化学卷(解析版) 题型:选择题
短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质。X原子最外层电子数是其内层电子数的3倍;Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性。下列说法正确的是
A. 原子半径: Z>X >Y
B. X元素形成的单质其摩尔质量一定是32g·moL -1
C. 物质A中既含离子键又含共价键
D. YX 2、ZX 2都有对应的含氧酸
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考四化学卷(解析版) 题型:选择题
下列关于下图所示转化关系(X代表卤素)的说法错误的是
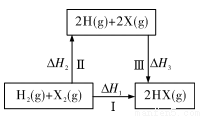
A.2H(g)+2X(g)==2HX(g) △H3<0
B.△H1=△H2+△H3
C.Cl、Br、I的非金属性依次减弱,所以按照途径I对应的△H1逐渐减小
D.途径I生成HC1放出的热量比生成HBr的多,说明HC1比HBr稳定
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上月考四化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是
A.在 NaHCO3溶液中:K+、Cl-、AlO2-、SO42-
B.加入铝粉能产生H2的溶液中:Na+、Fe3+、C1-、NO3-
C.c(OH-)/c(H+)=1012的溶液中:SO32-、NO3-、K+
D.含有大量 MnO4-的溶液中:H+、Ca2+、K+、C1-、C2O42-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A. 某试样焰色反应呈黄色,则试样中含有K+
B. 广泛pH试纸测得某碱性溶液的pH为12.5
C. 容量瓶不能用作溶解物质的容器
D. 粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上阶段测二化学卷(解析版) 题型:填空题
(1)用离子方程式解释:盛纯碱溶液的试剂瓶有玻璃塞,时间久了不易打开_____________。
(2)某同学想把AlCl3(aq)和Na2S(aq)混合制取A12S3,但最后得到一种白色絮状沉淀,而且混合液中有臭鸡蛋气味的气体放出。试解释造成此结果的原因,写出反应的离子方程式___________________。
(3)同温度下,具有相同 NH4+浓度的 NH3 ·H2O, NH4CI,CH3COONH4, NH4Fe(SO4)2 中,溶质浓度由大到小的顺序为_____________。
(4)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4C1溶液、盐酸和NaNO3溶液中的一种。己知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。则:B是 溶液,C是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com