
| A. | CH3CH(OH)CH3 | B. | CH3CH2OCH3 | C. | CH3CH2CH2OH | D. | CH3CH2CHO |
分析 结合有机物的相对分子质量为60,该有机物分子中有分子中含有C-H键、O-H键、C-O键;核磁共振氢谱显示该分子中有3个吸收峰,说明有3中不同的H原子,以此解答该题.
解答 解:A.CH3CH(OH)CH3相对分子质量为60,分子中含有C-H键、O-H键、C-O键,核磁共振氢谱有3个吸收峰,故A正确;
B.分子中不存在O-H键,故B错误;
C.分子中含有4个不同的H原子,则核磁共振氢谱有4个吸收峰,故C错误;
D.该有机物的相对分子质量是58,故D错误.
故选A.
点评 本题考查有机物的结构,为高频考点,侧重于学生的分析能力的考查,注意把握题给信息,把握有机物共价键种类的判断以及等效氢原子的识别,难度不大.


科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 其单质都能与水反应,通式为X2+H2O═HX+HXO | |
| B. | HX易溶于水,其水溶液都是强酸 | |
| C. | 其单质都有颜色,都有毒 | |
| D. | 最高价含氧酸的通式为HXO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
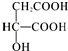 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 苹果酸中能发生酯化反应的官能团有2种 | |
| B. | 1 mol苹果酸可与3 mol NaOH发生中和反应 | |
| C. | 1 mol苹果酸与足量金属Na反应生成1 mol H2 | |
| D. | 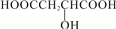 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 、
、 CH3CH═CHCHO+H2O
CH3CH═CHCHO+H2O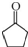 ,D中官能团的名称为碳碳双键、氯原子.
,D中官能团的名称为碳碳双键、氯原子. .
.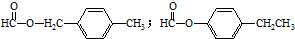 .
. )的合成路线:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{一定条件}{→}$
)的合成路线:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2$\stackrel{一定条件}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖能发生酯化反应 | |
| B. | 葡萄糖具有还原性 | |
| C. | 葡萄糖充分燃烧的产物为CO2与H2O | |
| D. | 完全燃烧等质量的葡萄糖和甲醛,所需氧气物质的量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 元素 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
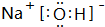 ; 属离子化合物(填“离子”或“共价”).
; 属离子化合物(填“离子”或“共价”). 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com