
【题目】如图所示,取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色.则下列说法错误的是( ) 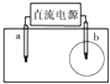
A.b电极是阴极
B.a电极与电源的正极相连
C.电解过程中水是氧化剂
D.b电极附近溶液的pH变小
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】工业上用某矿渣(主要成分是Cu2O,少量杂质是Al2O3、Fe2O3和SiO2)提取铜的操作流程如下: 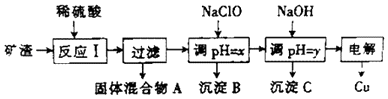
已知:①Cu2O+2H+═Cu+Cu2++H2O ②某些金属氢氧化物开始测沉淀和完全沉淀时的pH
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 2.2 | 5.8 |
沉淀完成pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)反应I中,与铁元素有关反应的离子方程式为、 .
(2)y的数值范围是
(3)以上步骤中的NaOH可以用代替(填字母)
A.CuO
B.NH4Cl
C.Cu(OH)2
(4)电解过程中,阳极产物可能为 .
(5)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,且该物质与还原产物的物质的量之比为4:1,该反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关丙烷、丙烯、丙炔说法中正确的有( )
A.丙烷、丙烯、丙炔的结构式分别为 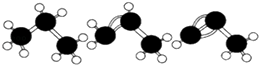
B.相同物质的量的三种物质完全燃烧,生成的气体在标准状态下,体积比3:2:1
C.丙烷、丙烯、丙炔三种物质的熔沸点逐渐升高,相对条件下密度逐渐增大
D.丙烷的碳原子空间结构是锯齿型的,不是简单的线性排列
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示仪器可用于实验室制备少量无水FeCl3 , 仪器连接顺序正确的是( ) 
A.a﹣b﹣c﹣d﹣e﹣e﹣f﹣g﹣h
B.a﹣e﹣d﹣c﹣b﹣h﹣i﹣g
C.a﹣d﹣e﹣c﹣b﹣h﹣i﹣g
D.a﹣c﹣b﹣d﹣e﹣h﹣i﹣f
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的电解池I和II中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d.符合上述实验结果的盐溶液是( )
选项 | X | Y |
A | MgSO4 | CuSO4 |
B | AgNO3 | Pb(NO3)2 |
C | FeSO4 | Al2 (SO4)3 |
D | CuSO4 | AgNO3 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL 0.01molL﹣1KCl溶液中,加入1mL 0.01molL﹣1AgNO3溶液,下列说法正确的是(已知AgCl Ksp=1.8×10﹣10)( )
A.有沉淀但不是AgCl
B.无AgCl沉淀
C.有AgCl沉淀析出
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示. 
回答下列问题:
(1)图B对应的物质名称是 , 其晶胞中的原子数为 , 晶体类型为 .
(2)d中元素的原子核外电子排布式为 .
(3)图A中由二种元素组成的物质中,沸点最高的是 , 原因是 , 该物质的分子构型为 , 中心原子的杂化轨道类型为 .
(4)图A中的双原子分子中,极性最大的分子是 .
(5)k的分子式为 , 中心原子的杂化轨道类型为 , 属于分子(填“极性”或“非极性”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙、丙三瓶等体积、等物质的量浓度的硫酸,若将甲用水稀释,在乙中加入少量BaCl2溶液,丙不变,然后分别与等浓度的NaOH溶液混合,至完全反应时,所消耗的NaOH溶液的体积是
A. 丙>乙>甲 B. 甲=丙>乙 C. 甲=丙=乙 D. 乙>丙>甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com