
| A. | 凑近集气瓶中闻氯气的气味 | |
| B. | 圆底烧瓶可以用酒精灯直接加热 | |
| C. | 金属钠着火时,用沙子扑灭 | |
| D. | 浓盐酸沾到皮肤上,用氢氧化钠溶液冲洗 |
分析 A、氯气有毒,把鼻子对着瓶口闻集气瓶中氯气的气味,容易导致中毒;
B、圆底烧瓶加热应垫石棉网;
C、钠、过氧化钠不与砂子反应;
D、氢氧化钠溶液具很强的腐蚀性.
解答 解:A、氯气有毒,直接闻氯气气味容易导致中毒,正确方法为:用手在试剂瓶瓶口轻轻煽动,让少量的气体加入鼻孔,故A错误;
B、圆底烧瓶加热应垫石棉网,不能用酒精灯直接加热,故B错误;
C、钠、过氧化钠不与砂子反应,所以金属钠着火后,可用砂子灭火,故C正确;
D、氢氧化钠溶液具很强的腐蚀性,所以不能用氢氧化钠冲洗,故D错误;
故选C.
点评 本题从生活的实际出发,考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力.


科目:高中化学 来源: 题型:选择题
| A. | 1 mol/L CaCl2溶液中含有Cl-的数目为NA | |
| B. | 标准状况下,2.24L HF所含分子数一定为0.1NA | |
| C. | 6.4g S6与S8的混合物中所含S原子数一定为0.2NA | |
| D. | 标准状况下,2.24L 氧元素的单质所含原子数一定为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③⑥ | C. | ②⑤⑥ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
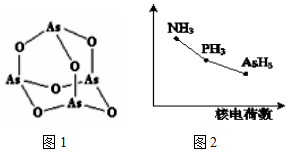
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
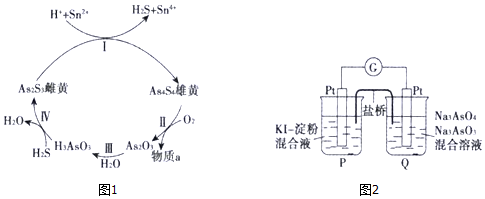
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 光化学烟雾的主要原因与排放SO2有关 | |
| B. | 工业上用二氧化硫来漂白纸浆、毛、丝、草帽、食品等 | |
| C. | 闪电时,大气中常伴有少量的NO2产生 | |
| D. | 正常雨水的PH小于5.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
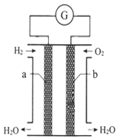 氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )
氢氧燃料电池是一种化学电源,如图所示,以石墨为电极,两极分别通入氢气和氧气,KOH溶液为电解质溶液,下列说法不正确的是( )| A. | 在电池反应中每转移2mol电子,正极消耗O2的体积为11.2L | |
| B. | b极的电极反应式为:O2+2H2O+4e-═4OH- | |
| C. | 工作一段时间后,电解质溶液碱性减弱 | |
| D. | 该装置将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 电解质溶液一定为强酸性 | |
| B. | 电子从a流出,经质子交换膜流向b | |
| C. | HS-在硫氧化菌作用下发生的反应为HS-+4H2O-8e-═SO42-+9H+ | |
| D. | 若该电池电路中有0.8mol电子发生转移,则有0.9molH+通过质子交换膜 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com