

分析 (1)①仪器c为滴液漏斗;
②在图A 装置中进行实验,向a中加入50mL0.5mol/LCuSO4溶液和100mL5mol/LNaOH溶液,振荡,再加入50mL40%的甲醛溶液,缓慢加热a,容器盛放液体不超过容积的$\frac{2}{3}$;
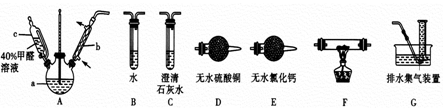
(2)为确认气体产物中含H2不含CO,装置A连接装置B除去甲醛,防止干扰后续实验验证,利用装置E吸收水蒸气,通过装置F中氧化铜加热反应,利用装置D中无水硫酸铜检验是否生成水蒸气,装置C中澄清石灰水检验是否生成二氧化碳验证气体中是否含一氧化碳,通过装置G收集剩余气体;
(3)甲醛被氧化为甲酸,甲酸被氧化为碳酸,若碱溶液中甲醛被氧化生成碳酸盐,加入浓盐酸会生成二氧化碳气体.据此设计实验验证;
(4)①氧化亚铜加入浓氨水得到无色溶液,在空气中变化为蓝色;
②锥形瓶ⅱ中固体完全溶解得深蓝色溶液是铜、氧气和一水合氨溶液反应生成深蓝色络离子;
③反应现象和元素守恒得到固体物质组成为氧化亚铜和铜,将容量瓶ⅱ中的溶液稀释100倍后,溶液的颜色与容量瓶ⅰ相近说明浓度相同.
解答 解:(1)①仪器c为(恒压)滴液漏斗,
故答案为:(恒压)滴液漏斗;
②在图A 装置中进行实验,向a中加入50mL0.5mol/LCuSO4溶液和100mL5mol/LNaOH溶液,振荡,再加入50mL40%的甲醛溶液,缓慢加热a,容器盛放液体不超过容积的$\frac{2}{3}$,计算得到容器容积最小为300ml,所以选择500ml三颈瓶较合适,故选C,
故答案为:C;
(2)为确认气体产物中含H2不含CO,装置A连接装置B除去甲醛,防止干扰后续实验验证,利用装置E吸收水蒸气,通过装置F中氧化铜加热反应,利用装置D中无水硫酸铜检验是否生成水蒸气,装置C中澄清石灰水检验是否生成二氧化碳验证气体中是否含一氧化碳,通过装置G收集剩余气体,依次连接的合理顺序为ABEFDCG,装置B的作用是吸收甲醛蒸气,防止其干扰后续检验,
故答案为:EFDC;吸收甲醛蒸气,防止其干扰后续检验;
(3)甲醛被氧化为甲酸,甲酸被氧化为碳酸,若碱溶液中甲醛被氧化生成碳酸盐,加入浓盐酸会生成二氧化碳气体.设计实验证明a中甲醛的碳元素未被氧化成+4价的方法为:取少量a中反应后的清液,滴入过量的浓盐酸,未见气泡产生,说明甲醛的碳元素未被氧化成+4价,
故答案为:取少量a中反应后的清液,滴入过量的浓盐酸,未见气泡产生,说明甲醛的碳元素未被氧化成+4价;
(4)①氧化亚铜加入浓氨水得到无色溶液,在空气中变化为蓝色,摇动锥形瓶ⅰ的目的是有利于溶液与空气中的氧气接触,
故答案为:有利于溶液与空气中的氧气接触;
②锥形瓶ⅱ中固体完全溶解得深蓝色溶液是铜、氧气和一水合氨溶液反应生成深蓝色络离子,反应的离子方程式为:2Cu+8NH3•H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O,
故答案为:2Cu+8NH3•H2O+O2=2[Cu(NH3)4]2++4OH-+6H2O;
③将容量瓶ⅱ中的溶液稀释50倍后,溶液的颜色与容量瓶ⅰ相近.由此可知固体产物的组成及物质的量之比约为n(Cu2O):n(Cu)=1:100,
故答案为:1:100.
点评 本题考查了物质组成的实验探究、物质性质、反应现象、实验关系分析判断,掌握基础是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | c(OH 一)>c(H +)时,a=b | B. | c(K +)>c(CH 3COO -)时,a>b | ||
| C. | c(OH 一)=c(H +)时,a>b | D. | c(K +)<c(CH 3COO-)时,a<b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当消耗CH3COOH的速率与消耗H2O2的速率相等时,反应达到限度 | |
| B. | 达反应限度时,CH3COOH、H2O2、CH3COOOH的浓度均不再变化 | |
| C. | 达反应限度时,CH3COOH不再与H2O2发生反应 | |
| D. | 若在反应中适当降低CH3COOH浓度,可提高反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的饱和HCOONa溶液、CH3COONa溶液的pH | HCOONa的pH<CH3COONa的pH | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向5ml2mol•L-1 NaOH溶液中加入1ml 1mol•L-1 CuSO4溶液,振荡后加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高铁酸钾(K2FeO4)是一种新型高效、多功能水处理剂,既能杀菌消毒又能净水 | |
| B. | “光化学烟雾”、“臭氧空洞”的形成都与氮氧化合物有关 | |
| C. | 用SO2漂白纸浆和草帽辫,该过程利用了SO2的氧化性 | |
| D. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol•L-1 r溶液的pH为2,s通常是难溶于水的液态混合物.上述物质的转化关系如下图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol•L-1 r溶液的pH为2,s通常是难溶于水的液态混合物.上述物质的转化关系如下图所示.下列说法正确的是( )| A. | 原子半径的大小W<X<Y | B. | 元素的非金属性Z>Y>X | ||
| C. | W、X形成的1:1型的化合物有很多种 | D. | X的最高价氧化物的水化物为强酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com