
| A、0.2 mol Na+ |
| B、0.05 mol CO |
| C、6.02×1023个 O |
| D、0.1 mol H |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、I2、SO32-、Cl-、Na+ |
| B、K+、Cu2+、OH-、NO3- |
| C、NH4+、Na+、Br-、SO42- |
| D、Ag+、NH3*H2O、NO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石墨转化为金刚石 |
| B、NaOH溶液与盐酸反应生成NaCl和H2O |
| C、NaCl熔化 |
| D、Na2O溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X离子的半径小于Y离子的半径 |
| B、X单质在空气中燃烧不止生成一种物质 |
| C、X、Y形成的化合物为共价化合物 |
| D、Y单质极容易与氢气发生化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子数之比等于2:3 |
| B、原子数之比等于2:3 |
| C、气体物质的量之比等于1:1 |
| D、质量之比等于7:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氨气通入醋酸溶液:CH3COOH+NH3═CH3COONH4 |
| B、亚硫酸氢钠溶液呈酸性:HSO3-+H2O?H3O++SO32- |
| C、氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| D、稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-═Ag++NO↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
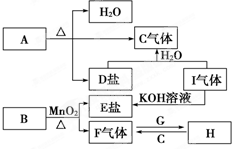 已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答:(提示:实验室制氧气可用氯酸钾与二氧化锰[作催化剂]混合加热制取)
已知A、B、C、D、E、F、G、H、I九种物质,其中A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G、F是单质,其余均为化合物,H是一种淡黄色固体,它们的转化关系如图所示.请回答:(提示:实验室制氧气可用氯酸钾与二氧化锰[作催化剂]混合加热制取)查看答案和解析>>
科目:高中化学 来源: 题型:
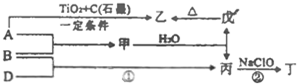 已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去).
已知:A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物.其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1mol丁分子中不同原子的数目比为1:2,且含有18mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用.各物质间的转化关系如图所示(某些条件已略去). 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com