
| A.Na+、K+、HCO3一、OH一 | B.Na+、H+、SiO32一、CO32一 |
| C.MnO4-、K+、Cl-、H+、SO42一 | D.Na+、SiO32一、OH一、Cl一 |


 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.氢氧化铁与硝酸 | B.澄清石灰水与盐酸 |
| C.烧碱与醋酸 | D.氢氧化钡与稀硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、K+、HCO3-、NO3- | B.NH4+、SO42-、Al3+、NO3- |
| C.Na+、Ca2+、NO3-、CO32- | D.K+、MnO4-、NH4+、NO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.①NaCl ②NaOH ③NH3·H2O ④H2SO4 |
| B.①NaCl ②NH3·H2O ③NaOH ④H2SO4 |
| C.①H2SO4②NaOH ③NH3·H2O ④NaCl |
| D.①H2SO4 ②NH3·H2O ③NaOH ④NaCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将水加热,Kw增大,pH不变 |
| B.NaHCO3溶液中存在6种分子或离子 |
| C.用25 mL碱式滴定管量取20.00mL高锰酸钾溶液 |
| D.用惰性电极电解足量的AgNO3溶液时,当有0.2 mole-转移时会析出21.6g银 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若c(OH-)>c(H+),a=b | B.若c(K+)<c(CH3COO-),a<b |
| C.若c(OH-)=c(H+),a>b | D.若c(K+)>c(CH3COO-),a>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、H+、CO32-、NO3- | B.Fe2+、Mg2+、Cu2+、Cl- |
| C.Ba2+、Cl-、NO3-、OH- | D.Mg2+、OH-、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
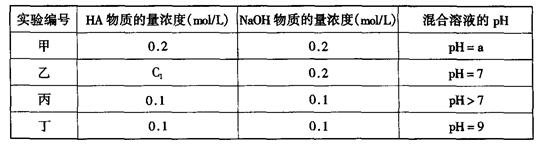 请回答:
请回答:| A.前者大 | B.后者大 | C.二者相等 | D.无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com