
【题目】华法林(Warfarin)又名杀鼠灵,为心血管疾病的临床药物。其合成路线(部分反应条件略去)如下所示:

回答下列问题:
(1)A的名称为________,E中官能团名称为________。
(2)B的结构简式为________。
(3)由C生成D的化学方程式为___________
(4)⑤的反应类型为_________,⑧的反应类型为________。
(5)F的同分异构体中,同时符合下列条件的同分异构体共有___________种。
a.能与FeCl3溶液发生显色反应 b.含有-CHO
【答案】甲苯 酯基 ![]() 2
2![]() +O2
+O2![]() 2
2![]() +2H2O 取代反应 加成反应 13
+2H2O 取代反应 加成反应 13
【解析】
根据④产物结构简式结合A分子式是C7H8可知,A结构简式为![]() ,A光照与Cl2发生取代反应生成B为
,A光照与Cl2发生取代反应生成B为![]() ,B发生水解反应生成C为
,B发生水解反应生成C为![]() ,C发生催化氧化生成D为
,C发生催化氧化生成D为![]() ,D与丙酮发生消去反应产生
,D与丙酮发生消去反应产生 ;苯酚与乙酸酐(CH3CO)2O发生取代反应产生E:
;苯酚与乙酸酐(CH3CO)2O发生取代反应产生E:![]() ,E在AlCl3、NaCl条件下加热发生反应产生F:
,E在AlCl3、NaCl条件下加热发生反应产生F:![]() ,F与
,F与![]() 在NaH存在时反应产生
在NaH存在时反应产生 ,
, 与
与 发生加成反应产生
发生加成反应产生 ,结合题目分析解答。
,结合题目分析解答。
根据上述分析可知:A为![]() ,B为
,B为![]() ,C为
,C为![]() ,D为
,D为![]() 。
。
(1)A为![]() ,A的名称为甲苯;E为
,A的名称为甲苯;E为![]() ,E中官能团名称为酯基。
,E中官能团名称为酯基。
(2)B的结构简式为![]() 。
。
(3)C为![]() ,C分子中羟基连接的C原子上含有2个H原子,可以在Cu催化下加热,发生氧化反应产生D:
,C分子中羟基连接的C原子上含有2个H原子,可以在Cu催化下加热,发生氧化反应产生D:![]() ,则由C生成D的化学方程式为:2
,则由C生成D的化学方程式为:2![]() +O2
+O2![]() 2
2![]() +2H2O。
+2H2O。
(4)苯酚与(CH3CO)2O发生取代反应产生E:![]() 和CH3COOH,所以⑤的反应类型为取代反应;
和CH3COOH,所以⑤的反应类型为取代反应; 与
与 发生加成反应产生
发生加成反应产生 ,故⑧的反应类型为加成反应。
,故⑧的反应类型为加成反应。
(5) F结构简式是![]() F的同分异构体符合下列条件:
F的同分异构体符合下列条件:
a. 能与FeCl3溶液发生显色反应,说明含有酚羟基;
b. 含有-CHO,能发生银镜反应。
如果取代基为-OH、-CH2CHO,有邻、间、对3种;
如果取代基为-OH、-CH3、-CHO,
-OH、-CHO相邻时有4种;
-OH、-CHO相间时有4种;
-OH、-CHO相对时有2种,
则符合条件的F的同分异构体的结构简式种类有:3+4+4+2=13种。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】根据表中![]() 部分短周期元素的原子半径及主要化合价
部分短周期元素的原子半径及主要化合价![]() 信息,判断以下叙述正确的是
信息,判断以下叙述正确的是
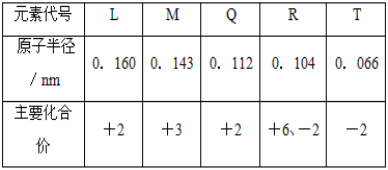
A.氢化物的沸点为![]()
B.L和Q的最高价氧化物对应的水化物的碱性![]()
C.M与T形成的化合物具有两性
D.![]() 与
与![]() 的核外电子数相等
的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作、现象与结论对应关系正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 相同温度下,同时向 ①4 mL 0.1 molL-1 KMnO4酸性溶液和②4 mL 0.2 molL-1 KMnO4酸性溶液中,分别加入4 mL 1 molL-1 H2C2O4溶液 | ①中溶液先褪色 | 该实验条件下,KMnO4浓度越小,反应速率越快 |
B | 向煤炉中灼热的煤炭上洒少量水 | 产生淡蓝色火焰,煤炭燃烧更旺 | 加少量水后,可使煤炭燃烧放出更多的热量 |
C | 加热2NO2(g) | 颜色加深 | 证明正反应是放热反应 |
D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH | 后者较大 | 证明非金属性 S>C |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是
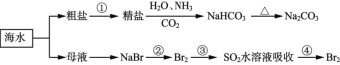
A.制取NaHCO3的反应是利用其溶解度小于NaCl
B.侯氏制碱应先通NH3再通CO2
C.在第②、③、④步骤中,溴元素均被氧化
D.③④的目的是进行溴的富集
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A(g)和2 mol B(g)在2 L的恒容密闭容器中混合并在一定条件下发生反应:2A(g)+B(g) 2C(g) ΔH<0,反应2 s后测得C的浓度为0.6 mol·L-1。下列说法正确的是
A.2 s后物质A的转化率为70%
B.当各物质浓度满足c(A)=2c(B)=c(C)时,该反应达到了平衡状态
C.达到平衡状态时,增加A的物质的量,A和B的转化率都提高
D.达到平衡状态时,升高温度,平衡逆向移动,同时化学平衡常数K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
1L海水在逐渐浓缩过程中析出盐的种类和质量(单位:g)的关系如下表所示:
海水密度(gmL-1) | CaSO4 | NaCl | MgCl2 | MgSO4 | NaBr |
1.21 | 0.05 | 3.26 | 0.004 | 0.008 | — |
1.22 | 0.015 | 9.65 | 0.01 | 0.012 | — |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 | 0.04 |
1.31 | — | 1.40 | 0.54 | 0.03 | 0.06 |
注:画“—”的数据少于10-4,可以忽略不计。
(1)从海水中获得粗盐,一般采用的方法是___。
(2)根据上表,要获得杂质较少的食盐,应控制海水的最佳密度为___gmL-1(填字母)。
A.1.21 B.1.22 C.1.26 D.1.31
(3)粗盐中常含有MgCl2、MgSO4、CaCl2等杂质,要除去这些杂质,按顺序加入的试剂依次为NaOH、BaCl2、___、___等(填化学式)。
(4)工业上电解熔融氯化钠制取金属钠的化学方程式为___。
(5)钠元素的一种常见氧化物可作为呼吸面具的供氧剂,写出该氧化物和CO2反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证氧化性:Cl2>Fe3+>SO2,某小组用图所示装置进行实验(夹持仪器和甲中加热装置已略,气密性已检验)。

实验步骤:
(1)在甲装置中,打开活塞a,加热,待装置中充满黄绿色气体时,与丙装置连接。
(2)当丙装置中FeC12溶液变黄时,停止加热。
(3)打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
(4)在乙装置中,打开活塞b,待空气排尽后,将乙中产生的气体通入上述丙装置变黄后的溶液中,一段时间后停止。
(5)更新丙中试管,打开活塞c,使约2mL的溶液滴入试管中,检验溶液中的离子。
回答下列问题:
(1)乙中发生反应的化学方程式为_________。
(2)实验中,证明氧化性Fe3+>SO2的离子方程式为_________。
(3)将甲装置与丙装置连接的目的是_______。
(4)有I、II、III三组同学分别完成了上述实验,实验结果如图:

上述实验结果一定能够证明氧化性:Cl2>Fe3+>SO2的是______(用“I”、“II”、“III”代号回答)。
(5)若要用以上甲和丙装置证明氧化性为:Cl2> Fe3+> I2的结论,则步骤为:
①往丙的漏斗中加入两种试剂____、___和一种溶剂_____。
②将甲装置中产生的Cl2慢慢通入丙中,观察丙的漏斗中溶液颜色变化。
③如果观察到丙中溶液________则结论正确。
④停止通入Cl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于工业合成氨反应:N2+3H2![]() 2NH3,下列说法错误的是( )
2NH3,下列说法错误的是( )
A.使用合适的催化剂可以加大反应速率B.升高温度可以增大反应速率
C.增大N2浓度可以使H2完全反应D.增大N2浓度可以增大反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依巴斯汀是一种抗过敏药物,羟基依巴斯汀(H)是该药物在人体中的初级代谢产物,其人工合成路线如下:
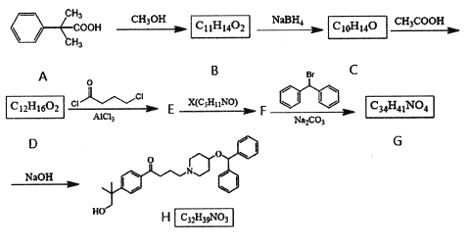
已知:
R-Cl![]() R-NH-R’
R-NH-R’
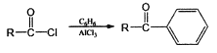
(1)F的结构简式为____________________
(2)下列说法不正确的是__________
A.l mol B可以和4 mol H2加成
B.X具有碱性
C.C可以发生取代、消去、加成等反应
D.1 mol E可以和3 mol NaOH反应
(3)写出由C生成D的反应方程式__________________________________________
(4)在F生成G过程中,Na2CO3的作用:___________________________________
(5)以苯和![]() 为原料合成
为原料合成![]() ,请设计出合成路径。___________
,请设计出合成路径。___________
(6)有机物Y的分子组成比X(C5H11NO)多1个“CH2”,写出三个满足下列条件的Y的同分异构体:________________________
①Y的分子中含有六元环状结构
②核磁共振氢谱表明Y分子中含有4种不同化学环境的氢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com