
【题目】(1)1mol H2SO4中含_____mol O 。4mol NH4NO3与______ mol H2SO4所含氧原子数相同。1.204×1024个Mg变成Mg2+失去____ mol eˉ。
(2)4.5g水与___________ g硫酸所含的分子数相等。
(3)乙醇(C2H6O)水溶液中,当乙醇分子和水分子中氢原子个数相等时,溶液中乙醇的质量分数为__________。
【答案】4 34 24.546%
【解析】
(1)1mol H2SO4中含4mol O 。4mol NH4NO3含12molO,与3mol H2SO4所含氧原子数相同。1molMg变成Mg2+失去2mol eˉ。
(2)分子数相等即物质的量相等。
(3)乙醇溶液中溶质的质量分数=乙醇质量/(乙醇质量+水的质量)×100%,因此需要判断溶质乙醇与溶剂水的质量关系;每个乙醇C2H5OH分子中含6个H原子,每个水H2O分子中含2个H原子;根据“乙醇分子里所含的氢原子总数与水分子里所含的氢原子总数相等”可推算溶液中乙醇与水的质量关系,然后计算出溶液中乙醇的质量分数.
(1)1mol H2SO4中含1mol×4=4mol O 。4mol NH4NO3与4mol ×3/4=3mol H2SO4所含氧原子数相同。1.204×1024个Mg变成Mg2+失去1.204×1024/6.02×1023mol-1 ×2=4 mol eˉ。
(2)4.5g水与98g·mol-1×4.5g/18g·mol-1 =24.5g硫酸所含的分子数相等。
(3)溶液中乙醇和水分子中含有氢原子数相等,根据乙醇和水的分子式可得乙醇分子与水分子间的关系:C2H5OH~6H~3H2O,则
C2H5OH~6H~3H2O
46 54
所以该乙醇溶液中溶质的质量分数为:![]() ×100%=46%。
×100%=46%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下图是某学生设计的实验室制备干燥Cl2及吸收多余氯气的实验装置图,请回答:
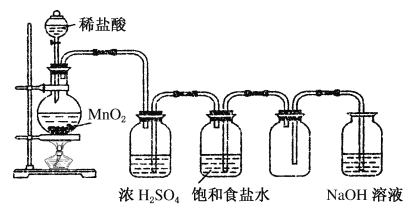
(1)指出上述图中的各处错误:
①_________________________________________________________;
②_________________________________________________________。
(2)在改过后的装置中,下列物质的作用分别是:
①饱和食盐水_________________________________________;
②浓硫酸____________________________________________;
③NaOH溶液_________________________________________。
(3)甲同学设计了如下图所示的实验装置并进行实验:
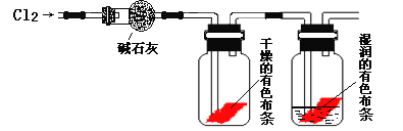
①甲同学实验后并没有得到预期的实验现象,请你帮助他分析实验失败的原因_____________________。
②甲同学在实验失败后对设计的实验装置进行了改进,并重新进行了实验,结果得到了预期的实验现象。你认为他预期的实验现象是______________________________________,由此得出Cl2使有色物质褪色的机理是________________________________________;
(4)如果将过量二氧化锰与20mL12mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06mol,其主要原因有①_______________________,②_____________________________。
(5)为了提高浓盐酸的利用率,你对该实验的建议是___________________________________。
(6)写出圆底烧瓶中发生反应的离子方程式__________________________________________。
实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是_________,有关的离子方程式是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(以让碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:

(1)灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是___________。
A.烧杯 B.表面皿 C.坩埚 D.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①___________,③___________。
(3)操作③中所用的有机试剂是CCl4,简述选择其理由_________________________________。
(4)操作过程③可以分解为如下几步:
A. 把盛有溶液的分液漏斗放在铁架台的铁圈中;
B. 把50 mL碘水和15 mL CCl4加入分液漏斗中,并盖好玻璃塞;
C. 检验分液漏斗活塞和上口玻璃塞是否漏液;
D. 倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E. 旋开活塞,用烧杯接收溶液;
F. 从分液漏斗上口倒出上层水溶液;
G. 将分液漏斗上口的玻璃塞打开或使玻璃塞上的凹槽或小孔对准分液漏斗口上的小孔;
H. 静置、分层。
a.正确操作步骤的顺序是(填写各操作的编号字母):______→______→_____→A→____→G→E→F。_____
b.上述G步操作的目的是:_________________________________;
c.最后碘的有机溶液是通过___________获得(填“漏斗上口”或“漏斗下口”)。
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:___________________。
(6)从含碘的有机溶液中提取碘和回收有机溶液,还需要经过蒸馏,观察下图所示实验装置,指出其所有错误之处__________________________________________。
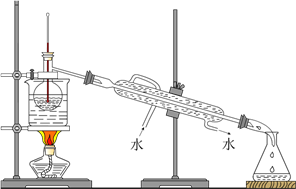
(7)进行上述蒸馏操作时,使用水浴的优点是_______________________________________,最后晶态碘在__________里聚集。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1869年门捷列夫制作第一张周期表的根据是依据原子序数,这在当时有重要意义。
B.周期表中有七个主族,八个副族,一个0族。18个纵行,共16个族。
C.短周期元素是指1~20号元素。
D.周期表中有七个周期。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A.在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原
B.得电子越多的氧化剂,其氧化性就越强
C.阳离子只有氧化性,阴离子只有还原性
D.有单质参加的反应不一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂(Pt)及其化合物用途广泛。
(1)在元素周期表中,铂元素与铁元素同族,则铂元素位于 ______。
A.s区 B.p区 C.d区 D.ds 区 E.f区
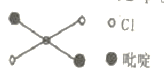
(2)二氯二吡啶合铂是由Pt2+ 、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同 分异构体。科学研究表明,反式分子和顺式分子一样具有抗癌活性。
①Cl-的外围电子排布式为 ______。
②吡啶分子是大体积平面配体,其结构简式如右图所示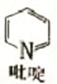 ,该配体的配位原子是_____。吡啶分子中,碳、氮原子的轨道杂化方式分别是 ___、____,各元素的电负性由大到小的顺序为_______。
,该配体的配位原子是_____。吡啶分子中,碳、氮原子的轨道杂化方式分别是 ___、____,各元素的电负性由大到小的顺序为_______。
③二氯二吡啶合铂分子中存在的微粒间作用力有 _____(填序号)。
a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键
④二氯二吡啶合铂分子中,Pt2+的配位数是4,但是其轨道杂化方式并不是sp3。简述理由: ________。
⑤反式二氯二吡啶合铂分子结构如图所示,该分子是 _____分子(选填“极性”、“非极性”)。
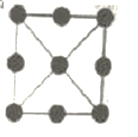
(3)金属铂立方晶胞沿 x、y或z轴的投影图如右图所示。若金属铂的密度为d g·cm-3,则晶胞参数a=_____nm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生取某物质溶于水,制得无色透明溶液,进行以下实验:①与碱反应生成盐和水;②与铁反应生成氢气;③该溶液中阳离子只有H+ . 根据你学过的酸的概念,其中能说明该物质为酸类物质的是( )
A.①②③
B.①②
C.②③
D.③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知食盐常加入KIO3来补充碘元素,检验食盐中是否加碘,可利用如下反应:
KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O
如果反应中转移0.2mol电子,则生成I2的物质的量为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有由等质量的NaHCO3和KHCO3组成的混合物a g,与100mL盐酸反应。(题中涉及的气体体积均以标准状况计,填空时可以用带字母的式子表示。)
(1)该混合物中NaHCO3与KHCO3的物质的量之比为__________________;
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸中HCl的物质的量为_____________mol;
(3)如果盐酸过量,生成CO2的体积为______________L;
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道_______________;
(5)若NaHCO3和KHCO3不是以等质量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积[V(CO2)]范围是________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com