
【题目】(1)药物安全是国家高度重视的民生问题,化学在新型药物的研究中贡献巨大。根据题意,用下列选项的字母代号填空。
A.阿司匹林(乙酸水杨酸) B.青霉素 C.抗酸药(氢氧化铝) D.麻黄碱
① 治疗胃酸过多,但患有严重的胃溃疡,应该选择_______;
② 可治疗支气管哮喘,但不宜过多服用(导致兴奋)的药物的是_______;
③ 是一种重要的抗生素类药,有阻止多种细菌生长的功能,该药物是_______;
④ 能使发热的病人体温降至正常,并起到缓解疼痛的作用,该药物是_______。
(2)2017年11月23日,国产大型喷气式客机C919首架机在航空工业试飞中心完成转场陕西阎良后的首次试飞,标志着C919向取得适航证并最终投入航线运营迈出关键一步。
①机身蒙皮使用的是第三代铝锂合金材料。下列不属于铝锂合金性质的是_______ (填字母)。

a.密度大 b.硬度大 c.抗腐蚀
②飞机轮胎属于橡胶制品。下列材料可用来合成橡胶的是_______ (填字母)。
a.石英砂 b.异戊二烯 c.石灰石
③机体先进复合材料的使用率达12%。下列属于复合材料的是_______ (填字母)。
a.钛合金 b.普通陶瓷 c.玻璃钢
(3)良好的生态环境和科学的饮食可以提升生活质量,根据题意,用下列选项的字母代号填空。
①臭氧层的破坏导致紫外线对地球表面辐射的增加,从而使全球皮肤癌的发病率明显增加。造成这一现象的主要原因是_______;
A.大量使用氟氯烃
B.炼钢时排放了大量高炉煤气
C.石油炼制厂排放了大量的甲烷、氢气
D.硝酸、硫酸工厂排放了大量的二氧化硫和一氧化氮
② 下列说法正确的是_______;
A.为使火腿肠颜色更鲜红,应多加一些亚稍酸钠
B.为摄取足够的蛋白质,应多吃肉、少吃豆制品
C.为减少室内甲醛污染,应提倡居室简单装修
D.为增强婴儿的食欲,应在婴儿食品中多加着色剂
③ 水体污染加剧了水资源的短缺。处理含Hg2+等重金属离子的废水常用的方法是_________;
A.沉淀法 B.中和法 C.蒸馏法 D.混凝法
【答案】 C D B A a b c A C A
【解析】(1)①治疗胃酸过多,但患有严重的胃溃疡,应该选择抗酸药(氢氧化铝),答案选C;②可治疗支气管哮喘,但不宜过多服用(导致兴奋)的药物的是麻黄碱,答案选D;③青霉素是一种重要的抗生素类药,有阻止多种细菌生长的功能,该答案选B;④阿司匹林(乙酸水杨酸)能使发热的病人体温降至正常,并起到缓解疼痛的作用,答案选A。(2)①铝锂合金具有密度小、硬度大和抗腐蚀等性能,答案选a;②异戊二烯可用来合成橡胶,答案选b;③a.钛合金属于合金,a错误;b.普通陶瓷属于无机非金属材料,b错误;c.玻璃钢属于复合材料,c正确,答案选c;(3)①A.氟氯代烃对臭氧层有很大的破坏作用,会使臭氧层形成空洞,从而使更多的紫外线照射到地球表面,导致皮肤癌的发病率大大增加,A正确;B.高炉煤气中含有二氧化硫,二氧化硫是导致酸雨的主要成分,B错误;C.石油炼制厂排放了大量的甲烷、氢气不会破坏臭氧层,C错误;D.二氧化硫、氮氧化物是形成酸雨的主要物质,氮氧化物还是形成光化学烟雾的罪魁祸首,所以硫酸、硝酸工厂排放了大量的二氧化硫和一氧化氮导致形成酸雨,D错误;答案选A。②A.亚硝酸钠有毒,A错误;B.豆制品富含蛋白质,B正确;C.甲醛有毒,危害人体健康,C错误;D.婴儿食品不能添加着色剂,D错误;答案选B;③处理含Hg2+等重金属离子的废水常用的方法是沉淀法,答案选A。


科目:高中化学 来源: 题型:
【题目】【选修5:有机化学基础】具有抗菌作用的白头翁素衍生物H的合成路线如图所示

已知: ①.RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
②.R﹣HC═CH﹣R′![]()
![]()
③.R﹣HC═CH﹣R′![]()

(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是____。C中官能团的名称是____。
(2)H的分子式为____,由G生成H的反应类型为____。
(3)试剂a的结构简式是____,试剂b为____。
(4)由C生成D的化学方程式是____。
(5)E与I2在一定条件下反应生成F的产物不唯一,此反应同时生成另外一种有机副产物且与F互为同分异构体,此有机副产物的结构简式是____。
(6)下列说法正确的是____。
A.E中含有3种官能团
B.1mol H与足量NaOH溶液反应,消耗2mol NaOH
C.由F生成G的反应是消去反应
D.1mol G最多可以与3mol H2发生加成反应
(7)与化合物C具有相同官能团且属于芳香族化合物的同分异构体共有____种(包括C本身)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( ) 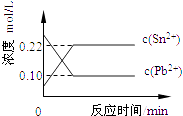
A.往平衡体系中加入金属铅后,c(Pb2+)增大
B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0
D.25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,八种短周期元素(用字母X表示)原子半径的相对大小、最高正价或最低负价的变化如图所示. 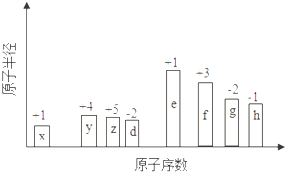
根据判断出的元素回答问题:
(1)y的元素名称 , 它位于元素周期表中第周期第族.
(2)h的最高价氧化物的化学式为 .
(3)d、g两种元素的最简单氢化物中稳定性比较强的物质,其结构式是 .
(4)x、z两元素可形成含有10个电子的分子,该分子的电子式为 . 位于第四周期且与z同主族的元素,其气态氢化物的化学式为 .
(5)e、f 两种元素最高价氧化物对应的水化物发生反应的离子方程式为 .
(6)将1mol e的单质在足量d 2中燃烧,所得产物中含有阴离子的数目为 , 含有的化学键为 . a.离子键 b.极性共价键 c.非极性共价键
(7)由x、d两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号) . a.MnO2 b.FeCl3 c.Na2SO3 d.K2SO4 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)我国利用海水制盐具有悠久的历史。目前,从海水中制得的氯化钠除食用外,还是重要的工业原料,从海水中生产金属钠流程如下。
![]()
请回答:
(1)③中反应的化学方程式是_____________________。
(2)若为了得到精盐,除去粗盐中含有杂质泥沙、Mg2+、Ca2+、SO42-等,则制备精盐的正确的操作顺序是________(填字母)。
a.将粗盐溶解 b.过滤 c.蒸发 d.加入过量的碳酸钠溶液 e.加入过量的氯化钡溶液f. 加入过量的氢氧化钠溶液 g. 加入盐酸,调溶液的pH略大于7
(3)在(2)中d操作的目的是______________________。
(4)若要制备2.3吨金属钠,理论上需要含质量分数为90%氯化钠的粗盐的质量是___吨。
(二)甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答下列问题:

(1)三位同学制取氨气的化学方程式是:_________________。
(2)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨气(实验操作都正确),你认为没有收集到氨气的同学是______(填“甲”、“乙”或“丙”)。
(3)为确定试管内是否已收集满氨气,应将湿润的红色石蕊试纸置于收集气体的试管口处,若观察到____________________,则说明氨气已收集满。
(4)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的的同学是______(填“甲”、“乙”或“丙”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2molL﹣1的一元酸HA与等浓度NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度所示,下列说法正确的是( ) 
A.HA为强酸
B.该混合溶液pH=7.0
C.该混合溶液中:c(A﹣)+c(Y)=c(Na+)
D.图中X表示HA,Y表示OH﹣ , Z表示H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com