
��15�֣�
��������ͭ�Ƚ������仯�������ճ�������Ӧ�ù㷺�����������ʵ��ش����⣺
��1������������ ���壬��FeCl3��Һ�������ɡ��������õ������� ���ѧʽ����
��2����д����������������Һ��Ӧ�Ļ�ѧ����ʽ____
��3������Cu�����백ˮ����˫��ˮ������Ӧ����������ߵĻ����Һ��Ӧ��������ɫ��Һ��������ɫ��Ũ��Һ�м����Ҵ��������������� ������������ɫ�����ӵĽṹʽ____ д��Cu�백ˮ��˫��ˮ��Ӧ�����ӷ���ʽ��____
��4��������������Һ�м��������̼����泥���FeCO3�������ɣ�д���仯ѧ����ʽ____
��15�֣�
��1���������壨1�֣���Fe2O3��2�֣�
��2��2Al��2NaOH��2H2O��2NaAlO2��3H2����3�֣�
��3����������ɫ���壨1�֣� 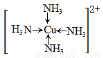 ��2�֣�
��2�֣�
Cu��4NH3��H2O��H2O2��[Cu(NH3)4]2����4H2O��2OH����3�֣�
��4��FeSO4��2NH4HCO3��FeCO3����CO2����(NH4)2SO4��H2O��3�֣�
��������
�����������1���������ǽ������壻FeCl3����ˮ�����������������Ȼ��⣬�Ȼ����ӷ������Լ��ȴ�ʹˮ��ƽ��һֱ�����ƶ����������������������������������ֽ����������������Խ�FeCl3��Һ�������ɡ��������õ�������Fe2O3��
��2����������������Һ��Ӧ�Ļ�ѧ����ʽΪ2Al��2NaOH��2H2O��2NaAlO2��3H2����
��3������ɫ��ҺΪ�������İ���ͭ����Һ�����뼫�Խ�С���ܼ��Ҵ���������ɫ����������������ɫ������[Cu(NH3)4]��OH��2��������ɫ��������[Cu(NH3)4]2������ṹʽΪ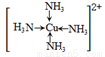
��������Ϣ��֪Cu�백ˮ��˫��ˮ��Ӧ�����������İ���ͭ��Һ�����Ի�ѧ����ʽΪCu��4NH3��H2O��H2O2��[Cu(NH3)4]2����4H2O��2OH��
��4��������������Һ�м��������̼����泥���FeCO3�������ɣ�˵������������̼��������ӷ���˫ˮ�ⷴӦ���仯ѧ����ʽΪFeSO4��2NH4HCO3��FeCO3����CO2����(NH4)2SO4��H2O
���㣺������������ͭ���仯����Ļ�ѧ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2013-2014������5�¸����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
��17�֣����տ�ѧ�����з����л��ϳ��е��ٴ��Ľ���ż���������2010���ŵ������ѧ�����л��ϳɳ��õ���/����̿��������ʹ�ã������ᱻ���ʣ��磺�����л���ȣ���Ⱦ��ʧȥ���ԣ���Ϊ�ϴ��������������������á�һ���ɷϴ�����ȡ�Ȼ���(PdCl2)�Ĺ����������£�
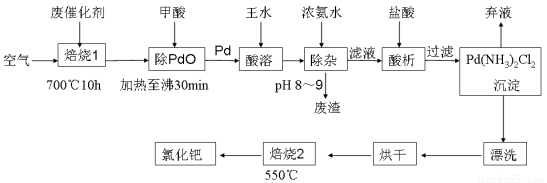
��1�����ỹԭ�����ٵĻ�ѧ����ʽΪ�������� ������������ ��
��2����Ũ��ˮʱ����Ԫ��ת��Ϊ������[Pd(NH3)4]2+����ʱ��Ԫ�صĴ�����ʽ�ǡ���������д��ѧʽ����
��3����ˮ��Ũ������Ũ���ᰴ�����1��3��϶��ɵģ�������ˮ���ܽ�Ĺ������л�����A��һ����ɫ���ж�����B���ɡ�
��������B�Ļ�ѧʽΪ��������
���ھ��ⶨ��������A��3��Ԫ����ɣ��й�Ԫ�ص���������ΪPd��42.4%��H��0.8%����A�Ļ�ѧʽΪ����
��4���ٵĻ����ʸߵ���Ҫȡ������ˮ�ܽ�IJ�����������֪��Ӧ�¶ȡ���Ӧʱ�����ˮ�������ٻ����ʵ�Ӱ����ͼ1��ͼ3��ʾ������ˮ�ܽ��ٵ����������ǣ���Ӧ�¶�Ϊ�� ����Ӧʱ��ԼΪ�� �����ٵ���Ʒ����ˮ��������Ϊ���� ������ ��
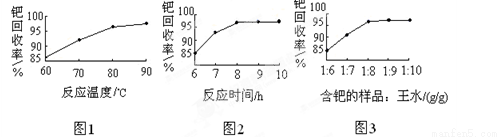
��5��700�桰����1����Ŀ���ǡ������� �� 550�桰����2����Ŀ���ǡ������������������������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������У����5�µ���������Կ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
4�ֶ�����Ԫ��W��X��Y��Z��ԭ����������������ԭ�ӵ�����������֮��Ϊ19��W��XԪ��ԭ����������֮��Ϊ1��2��X2+��Z�����ӵĵ�����֮��Ϊ8������˵������ȷ����
A����W���ڵ�ͬ����Ԫ�ؿ��Ƴ���Ҫ�İ뵼�����
B��Ԫ��ԭ�Ӱ뾶�Ӵ�С��˳����X��Y��Z
C��WZ4������W��Zԭ��ͨ�����ۼ�������������ﵽ8���ӽṹ
D��W��Y��ZԪ�ض�Ӧ���⻯���ȶ�����ǿ����H2Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ѧ�ڸ����ڶ�����ϲ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
(15��)ij��ѧ��ȤС���������¸�װ�����ӳ�һ����װ�ã�̽�������백��֮��ķ�Ӧ������DΪ��������������봿�����ﰱ����Ӧ��װ�ã�
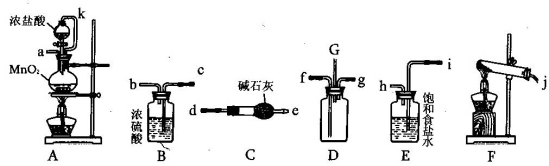
��ش��������⣺
(1)���Ӻ�װ�ú�����е�һ��ʵ�������__________________
(2)װ��E��������____________����k��������________________________
(3)��װ��D��G���ݳ���β���п��ܺ��л���ɫ���ж����壬����������__________________
(4)װ��F���Թ��ڷ�����Ӧ�Ļ�ѧ����ʽ____________________________________
(5)����Dװ�õ�����������߽ϳ����ұ߽϶̣�Ŀ����______________________________
(6)����װ�ô������ҵ�����˳����(j)��( ) ( )��(f) (g)��( ) ( )��( ) ( )��(a)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014��������ѧ�ڸ����ڶ�����ϲ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������˵����ȷ����
A���ڷ�Ӧ������1mol Cl2��ת�Ƶĵ�����һ��Ϊ2NA��
B����״���£�0.5mol�������еĵ�����ΪNA
C��15g CH3+(̼������)�к��е�����Ϊ10NA
D��0.1L 2mol��L��1��(NH4)2S��Һ�к��е�S2����ĿΪ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014������������������ǰģ�����ۻ�ѧ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A��lmol Cl2ͨ�뺬��2mol FeI2����Һ�У�2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
B������ʯ��ˮ������С�մ���Һ��ϣ�Ca2++OH-+ HCO3-=CaCO3��+H2O
C��AlCl3��Һ�м��������ˮ��Al3++4 OH-= AlO-2+2H2O
D����������Һ�м������������[Ag(NH3)2]++OH-+3H+= Ag++2NH4++ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и߶���ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��(NH4)2SO4��CuSO4��Һ����ʹ�����ʳ�������
B���������ȩ���������������ɷ�ȩ��֬�Ľṹ��ʽΪ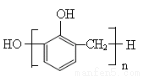
C�������Ӳ֬�ụΪͬϵ�C6H14��C9H20Ҳһ����Ϊͬϵ��
D��Ҷ��ĽṹΪ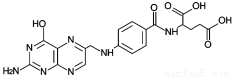 �������Է���������ˮ�⡢�ӳɵȷ�Ӧ
�������Է���������ˮ�⡢�ӳɵȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����һ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ԭ������֪��HClΪǿ�ᣬ���жԱ�ʵ�鲻������֤��CH3COOHΪ�������
A���Աȵ�Ũ�ȵ��������pH
B���Աȵ�Ũ�ȵ������ᣬ����ͬ��Сþ����Ӧ�ij�ʼ����
C���Աȵ�Ũ�ȡ�������������ᣬ�����NaOH��Һ��Ӧ��ų�������
D���Աȵ�Ũ�ȡ�������������ᣬ������Zn��Ӧ������H2�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014����ʡ����������������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
������һ���ḻ���ʱ��⣬ͨ����ˮ���ۺ����ÿɻ���������ʹ�����ʹ�á�
��1����ˮ���εĿ������ã�
�ٺ�ˮ����Ŀǰ�����Ϊ�������������ѡ��Զ�뽭���뺣�ڣ�������꣬��ϫ��������ƽ̹�տ��ĺ�̲�����������Ϊ��ˮ�ء������غ� �ء�
��Ŀǰ��ҵ�ϲ��ñȽ��Ƚ������ӽ���Ĥ���۷������ȼҵ�������ڵ����������ӽ���Ĥֻ����������ͨ������ֹ�����Ӻ�����ͨ������˵���ȼ������������ӽ���Ĥ�����ã� ��дһ�㼴�ɣ���
��2�����������ǽ��귢չ���һ�ֽϺõĺ�ˮ������������ԭ����ͼ��ʾ�����о���ѡ���Ե������ӽ���Ĥ�������ӽ���Ĥ������С���ش���������⣺
�ٺ�ˮ����ֱ��ͨ�뵽�������У������� ��
��A���ų����� �����ˮ����Ũˮ������
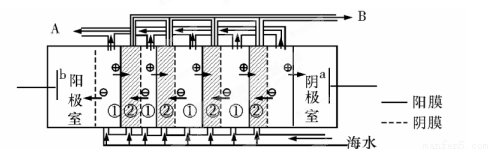
��3���ÿ�±����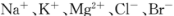 �����ӣ�����ȡ�壬�������������£�
�����ӣ�����ȡ�壬�������������£�

�����������е���Һ��BrO3-�����������з�Ӧ�����ӷ���ʽΪ�� ��
��ͨ�����Ȼ��ѻ�ú�Br2����Һ��Ϊ�λ��辭�����������ա��ữ���»�ú�Br2����Һ�� ��
������������ͨ��ˮ�������ȣ������¶���90�����ҽ��������ԭ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com