
 2SO3������Ӧ���ʷֱ���v��SO2����v��O2����v��SO3����mol��L��1��min��1����ʾ���淴Ӧ���ʷֱ���v�䣨SO2����v�䣨O2����v�䣨SO3����mol��L��1��min��1����ʾ������Ӧ�ﵽ��ѧƽ��ʱ����ȷ�Ĺ�ϵ��
2SO3������Ӧ���ʷֱ���v��SO2����v��O2����v��SO3����mol��L��1��min��1����ʾ���淴Ӧ���ʷֱ���v�䣨SO2����v�䣨O2����v�䣨SO3����mol��L��1��min��1����ʾ������Ӧ�ﵽ��ѧƽ��ʱ����ȷ�Ĺ�ϵ�� v�䣨SO2��
v�䣨SO2��| A���٢ڢۢ� | B���٢ڢ� | C���ڢۢ� | D���٢� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ���� | X | Y | Z |
| ��ʼ���ʵ���(mol) | 0.2 | 0.2 | 0 |
| ƽ�����ʵ���(mol) | 0.1 | 0.05 | 0.1 |
 2Z����ƽ�ⳣ��Ϊ8 000
2Z����ƽ�ⳣ��Ϊ8 000�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)����H<0��4 s��Ӧ�ﵽƽ��״̬����ʱ���C��Ũ��Ϊ0.6 mol/L������˵����ȷ����(����)
2C(g)����H<0��4 s��Ӧ�ﵽƽ��״̬����ʱ���C��Ũ��Ϊ0.6 mol/L������˵����ȷ����(����)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)��D(s)������˵����ȷ����(����)
2C(g)��D(s)������˵����ȷ����(����)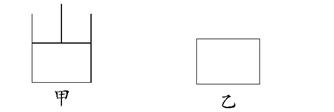
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2A2B(g)����Ӧ�ﵽƽ��ʱA2BΪ0.3 mol������ʱ����0.5 mol A2��0.5 mol B2�������´ﵽƽ���A2B�����ʵ���(����)
2A2B(g)����Ӧ�ﵽƽ��ʱA2BΪ0.3 mol������ʱ����0.5 mol A2��0.5 mol B2�������´ﵽƽ���A2B�����ʵ���(����)| A������0.3 mol |
| B������0.15 mol |
| C����0.15 mol |
| D������0.15 mol����0.3 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO2��g��+ O2��g�� 2SO3��g�������С�H < 0 ������Ӧ�ﵽƽ��ʱ������λ����ͼ2��ʾ��
2SO2��g��+ O2��g�� 2SO3��g�������С�H < 0 ������Ӧ�ﵽƽ��ʱ������λ����ͼ2��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
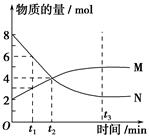
A����ѧ����ʽΪ��2M N N |
| B��t2ʱ�����淴Ӧ������ȣ��ﵽƽ�� |
| C��t3ʱ������Ӧ���ʴ����淴Ӧ���� |
| D��t1ʱ��N��Ũ����MŨ�ȵ�2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��һ�������£�2molsO2������O2��Ӧ�ɵõ�2molsO3 |
| B����4mol HCl��Ũ������������MnO2���ȷ�Ӧ���Ʊ�1mol Cl2 |
| C��10mL 18.0mol/L H2SO4������ͭ���ȷ�Ӧ���Ʊ�0.09molsO2 |
| D��һ�������£�1mol N2��3mol H2��Ӧ���Ʊ�1.0mol NH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NO2(g)��ǰ110 s�ڵķ�Ӧ��������������ͼ��ش��������⡣
2NO2(g)��ǰ110 s�ڵķ�Ӧ��������������ͼ��ش��������⡣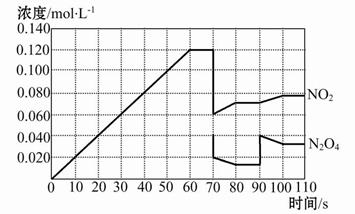
| A��������� | B������������� |
| C�������¶� | D������N2O4��Ũ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com