
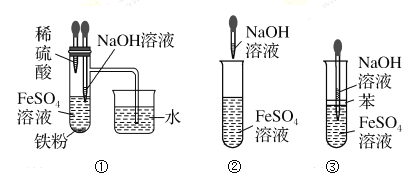
【题目】下列各图示中能较长时间看到Fe(OH)2白色沉淀的是( )
A.①②B.①③C.②③D.①②③
【答案】B
【解析】
能较长时间看到Fe(OH)2白色沉淀,则制备实验装置应排出空气,防止氢氧化亚铁被氧化,以此来解答。
因为Fe(OH)2在空气中易被氧化成Fe(OH)3,故要长时间观察到Fe(OH)2白色沉淀,就要排除装置中的空气或氧气。装置①是先用Fe粉与稀硫酸反应产生的H2将装置中的空气排尽,然后滴入NaOH溶液,与新反应产生的FeSO4发生复分解反应制取Fe(OH)2,并使生成的Fe(OH)2处在氢气的保护中,可以达到目的,①正确;
②滴入的NaOH溶液会吸收空气中的氧气,与试管中FeSO4发生复分解反应制取Fe(OH)2和Na2SO4,溶液中有氧气,会氧化Fe(OH)2变为Fe(OH)3,因此会看到沉淀由白色迅速变为灰绿色,最后变为红褐色,不能达到实验目的,②错误;
③中液面上加苯阻止了空气进入;在隔绝空气的环境中NaOH、FeSO4发生复分解反应产生Fe(OH)2和Na2SO4,由于没有空气,Fe(OH)2不能被氧化,能较长时间观察到白色沉淀,③正确;
故合理选项是B。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】如图是硫酸试剂标签上的部分内容,据此下列说法正确的是( )

A.该硫酸试剂的物质的量浓度为18.4mol·L-1
B.该硫酸可以干燥H2S等酸性气体,但不可以干燥NH3
C.50mL该H2SO4中加入足量的铜片并加热,被还原的H2SO4的物质的量为0.46mol
D.2.7gAl与足量的该硫酸反应可得到H23.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g) == 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1
(2)C(s)+ O2(g) == CO2(g) △H2=-393.5 kJmol-1
(3)H2(g) +![]() O2(g) == H2O(l) △H3=-285.8kJ·mol-1
O2(g) == H2O(l) △H3=-285.8kJ·mol-1
则反应2C(s)+2H2(g) +O2(g) == CH3COOH(l)的△H为( )
A. -488.3 kJ·mol-1 B. -244.15 kJ·mol-1 C. +488.3 kJ·mol-1 D. +244.15 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
A.1.8 g NH4+中含有的电子数为1.1NA
B.2.2 g CO2和N2O的混合气体中原子数为0.15NA
C.1 mol Na2O2与足量CO2反应,转移电子数为2NA
D.25 ℃、101 kPa时,2.24 L CH4含有的质子数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 100g质量分数为 46%C2H5OH溶液中所含O—H数目约为7NA
B. 质量为12g的12C含有的中子数为12NA
C. 将0.1molCH3COONa溶于稀醋酸中使溶液呈中性,溶液中CH3COO-数目小于0.1NA
D. 氢氧燃料电池正极消耗22.4 L气体时,电路中通过的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,向2L恒容密闭容器中充入1mol NO2与2mol SO2发生如下反应:NO2(g)+SO2(g) ![]() SO3(g)+NO(g)△H=﹣41.8kJ/mol。
SO3(g)+NO(g)△H=﹣41.8kJ/mol。
(1)下列能说明该反应达到平衡状态的是_____________。
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗n mol SO3的同时生成n mol NO2
(2)反应进行到20s 时,测得反应速率v(NO)=0.005mol/(Ls) , 则消耗的NO2为_____mol。
(3)下列措施能使反应加快的是___(仅改变一个条件)
a.降低温度 b.缩小容积 c.使用效率更高的催化剂
(4)若上述容器为绝热容器(与外界无热交换),则到达平衡所需时间将__________。
a.延长 b.缩短 c.不变 d.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物分子中的碳碳双键发生臭氧氧化反应: ,有机物A的结构简式为
,有机物A的结构简式为 ,G的分子式为C7H12O,以下A~H均为有机物,其转化关系如下:
,G的分子式为C7H12O,以下A~H均为有机物,其转化关系如下:

(1)下列说法正确的是 ______ 。(填字母序号)
A.C的官能团为羧基
B.1molA最多可以和2molNaOH反应
C.C可以发生氧化反应、取代反应和加成反应
D.![]() 可以发生消去反应
可以发生消去反应
(2)F的结构简式为____________ ,由F到G的反应类型为___________ 。
(3)反应①的作用是__________________ ,合适的试剂a为____________。
(4)同时满足下列条件的A的一种同分异构体的结构简式______________________。
Ⅰ.与A具有相同的官能团;Ⅱ.属于苯的邻二取代物;Ⅲ.能使FeCl3溶液显色;Ⅳ.核磁共振氢谱分析,分子中有8种不同化学环境的氢原子。
(5)H与G分子具有相同的碳原子数目,且1molH能与足量的新制银氨溶液反应生成4mol单质银。写出H与足量的新制银氨溶液反应的化学方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.84 g的铜加入100 mL H2SO4和HNO3混合液中,铜全部溶解并放出无色气体。向溶液中加入2.70 g铝粉,充分反应后过滤,得到溶液X、滤渣Y和气体Z,气体Z遇空气不变色,在标准状况下的体积为672 mL。下列说法正确的是
A. 溶解铝粉的质量为0.54 g
B. 滤渣Y中可能只含有Cu
C. 原混合液中的c(H2SO4):c(HNO3)=9:4
D. 若向溶液X中加入100 mL 2.0 mol·L-1氢氧化钠溶液,充分反应,所得沉淀为4.68 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度、体积的密闭容器中,可逆反应A(s)+3B(g)![]() 2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
2C(g)达到平衡时,下列说法能判断该反应达到平衡的是( )
①C的生成速率和C的分解速率相等
②单位时间内生成amolA,同时生成3amolB
③混合气体的密度不再变化
④混合气体的总压强不再变化
⑤A、B、C物质的量之比为1∶3∶2
⑥混合气体的平均相对分子质量不变
⑦容器中C的体积分数不变
A.②④⑤⑦B.①③④⑥⑦C.①④⑥⑦D.①③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com