
| A. | 核外电子数为奇数的基态原子,其原子轨道中一定不含有“未成对电子” | |
| B. | 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” | |
| C. | 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” | |
| D. | 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子” |
分析 主族元素除最外层以外的各内层电子都是成对的,最外层为nsx或ns2npy,s能级只有1个轨道最多容纳2个电子,p能级含有3个简并轨道,电子排布在同一能级的各个轨道时,优先占据不同的轨道,如两电子占据np轨道分别占据两个轨道,形成两个未成对电子,结合选项讨论最外层电子数,根据核外电子排布规律分析.
(注意:s p d f 能级所含轨道数分别为1、3、5、7,均为奇数,而电子排布在同一能级的各个轨道时,优先占据不同的轨道,每个轨道最多容纳2个电子,故核外电子总数为奇数一定具有未成对电子,为偶数可能含有未成对电子,也可能没有未成对电子).
解答 解:A.核外电子数为奇数的基态原子,则原子最外层电子数为奇数,若最外层为nsx,则x=1,含有未成对电子;若最外层为ns2npy,则y=1或3或5,np轨道一定含有未成对电子,故A错误;
B.核外电子数为偶数的基态原子,若最外层为ns2npy,则y=2或4,np轨道一定含有未成对电子,如14号硅原子,最外层为3s23p2,3p两个电子未成对,故B错误;
C.偶数族元素的基态原子,若最外层为nsx,则x=2,不含有未成对电子,如12号镁原子,最外层为3s2,若最外层为ns2npy,则y=2或4,np轨道含有未成对电子,所以其原子轨道中可能含有“未成对电子”,故C正确;
D.奇数族元素的基态原子,则原子最外层电子数为奇数,若最外层为nsx,则x=1,含有未成对电子;若最外层为ns2npy,则y=1或3或5,np轨道一定含有未成对电子,故D错误.
故选C.
点评 本题考查核外电子排布规律、主族元素的核外电子排布特点等,理解核外电子排布规律是解答关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2 | |
| B. | 1 mol CO+1mol H2O(g)+1mol CO2+1mol H2 | |
| C. | 0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4mol H2 | |
| D. | 0.5mol CO+1.5mol H2O(g)+0.5mol CO2+0.5mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
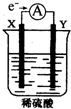 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A. | X极上发生的是还原反应 | |
| B. | 若两电极分别为Fe和碳棒,则Y为Fe | |
| C. | 若反应进行一段时间后,产生2克H2时转移了1mol电子 | |
| D. | 溶液中的SO42-向X极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④⑤ | B. | 只有①③④ | C. | 只有①②③⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO3已部分被空气中的氧气氧化 | |
| B. | 加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 | |
| C. | 题中操作可证明Na2SO3溶液是否被氧化 | |
| D. | 此实验不能确定Na2SO3是否部分被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为53、中子数为78的碘原子:${\;}_{53}^{131}$I | |
| B. | N2的电子式: | |
| C. | S2-的结构示意图: | |
| D. | 甲烷分子的比例模型是 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若将产物通过碱石灰,则不能被完全吸收 | |
| B. | 若将产物通过浓硫酸,充分吸收后,浓硫酸增重18g | |
| C. | 产物的平均摩尔质量为24g.mol-1 | |
| D. | 反应中消耗O256g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 131I 原子的中子数为78 | B. | 131I 与127I互为同素异形体 | ||
| C. | 核裂变是一种化学变化 | D. | 碘在周期表中位于第四周期ⅦA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com