
【题目】Ⅰ.实验室利用铜和稀硝酸制备一氧化氮:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,该反应的离子方程式为___。每生成11.2LNO(标准状况),转移的电子数为___NA。
Ⅱ.(1)在发射“神舟”十一号的火箭推进器中装有肼(N2H4)和过氧化氢,当两者混合时即产生气体,并放出大量的热。已知:
N2H4(l)+2H2O2(l)==N2(g)+4H2O(g) ΔH1;
H2O(l)==H2O(g) ΔH2
请写出液态肼与足量过氧化氢反应生成氮气和液态水的热化学方程式:_____。
(2)在25℃,101kPa下,1molCO完全燃烧放出283.0kJ的热量。请写出表示CO燃烧热的热化学方程式:___。
【答案】3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 1.5 N2H4(l)+2H2O2(l)=N2(g)+4H2O(l) ΔH=ΔH1-4ΔH2 CO(g)+ ![]() O2(g)=CO2(g) ΔH=-283.0 kJ/mol
O2(g)=CO2(g) ΔH=-283.0 kJ/mol
【解析】
I. 铜和稀硝酸反应,稀硝酸、硝酸铜可拆为离子形式,可写出其离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,每生成标况下11.2LNO,即生成0.5molNO,转移的电子数为1.5 NA;
II. (1)液态肼与足量过氧化氢反应生成氮气和液态水的方程式为N2H4(l)+2H2O2(l)=N2(g)+4H2O(l),根据盖斯定律,该式可由题目中的上式-4倍的下式得到,即该反应的ΔH=ΔH1-4ΔH2,故热化学方程式为N2H4(l)+2H2O2(l)=N2(g)+4H2O(l) ΔH=ΔH1-4ΔH2;
(2)燃烧热为1mol可燃物完全燃烧生成稳定物质时放出的能量,故表示CO燃烧热的热化学方程式为CO(g)+ ![]() O2(g)=CO2(g) ΔH=-283.0 kJ/mol。
O2(g)=CO2(g) ΔH=-283.0 kJ/mol。


科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe2O3的混合物中,加入500 mL 1 mol/L的盐酸,恰好使混合物完全溶解,放出672 mL(标准状况)气体。向所得溶液中加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,能得到铁( )
A. 28 g B. 14 g
C. 12.32 g D. 条件不足,无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。

(1)请根据甲同学的示意图,所需实验装置从左至右的连接顺序:装置②→__________。
(2)装置②中主要玻璃仪器的名称__________、__________、__________。
(3)实验室制备Cl2的离子方程式为____________。
(4)装置③中Cu的作用__________(用化学方程式表示)。
(5)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入__________。
(6)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到__________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸二氢钾(KH2PO4)是一种重要的化工产品,工业上常用作缓冲剂和培养剂,农业上常用作 复合肥料。以氟磷灰石[主要成分为Ca5F(PO4)3,还含有少量的Fe2O3、A12O3等杂质]为原料制备KH2PO4 晶体的一种流程如下:
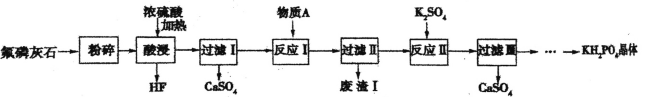
回答下列问题:
(1)“酸浸”过程中生成磷酸的化学方程式为________,若用盐酸代替硫酸,磷酸的产率会明显提高,原因是___,该过程所用的仪器不能釆用二氧化硅陶瓷材料,其主要原因是_____________(用化学方程式表示)。
(2)己知物质A为CaCO3,其作用是调节溶液pH,则“废渣I”的主要成分为__________。
(3) “反应II ”的化学方程式为 _______。
(4)将获得的KH2PO4晶体进行进一步提纯的方法名称为____。
(5)若用1000kg质量分数为50.4%的氟磷灰石来制取磷酸二氢钾晶体,其产率为80%,则生产出的磷酸二氢钾晶体的质量为 _____kg. 已知摩尔质量 M(Ca5F(PO4)3)=504g/mol,M(KH2PO4)=136 g/mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列比较中,正确的是:
A. 常温下,pH=11的Na2CO3溶液中,水电离出的c(OH-)=1.0×10-3molL-1
B. 同温度同物质的量浓度时,HF比HCN易电离,则NaF溶液的pH比NaCN溶液的大
C. 物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-)
D. 加热蒸干AlCl3溶液可得到AlCl3固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,CH3COOH的电离常数Ka=1.8×10-5。常温下,往25mL氢氧化钠标准溶液中逐滴加入0.1mol·L-1的CH3COOH溶液,pH变化曲线如图所示:
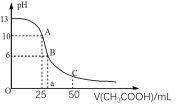
(1)该氢氧化钠溶液的物质的量浓度为__。
(2)A点对应的横坐标为25mL,请用离子方程式解释A点所示的溶液显碱性的原因:__。
(3)A点所示的溶液中各离子浓度由大到小的排列顺序是:______。
(4)B点所示溶液中,![]() =___。
=___。
(5)C点所示溶液为等浓度的CH3COONa和CH3COOH混合溶液,请判断该溶液中c(CH3COOH)__c(CH3COO-)。(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】螺[2,2]戊烷的结构简式如图。下列关于该化合物的说法错误的是( )

A.与环戊烯互为同分异构体B.二氯代物超过两种
C.所有碳原子不共平面D.与丙烷互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1的MOH溶液,如中所示曲线表示混合溶液的pH变化情况。下列说法中正确的是( )
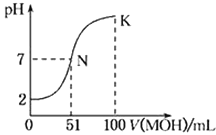
A.HA为一元弱酸,MOH为一元强碱
B.滴入MOH溶液的体积为50 mL时,c(M+)>c(A-)
C.N点水的电离程度大于K点水的电离程度
D.K点时,c(MOH)+ c(M+)=0.02 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.二氧化硅溶于氢氟酸溶液中: SiO2+4H++4F-=SiF4↑ +2H2O
B.偏铝酸钠溶液中通入过量的CO2:2AlO2- + CO2+3H2O=2Al(OH)3↓+ CO32-
C.稀硫酸加入氢氧化钡溶液中:H+ +![]() + Ba2+ + OH-=BaSO4↓+ H2O
+ Ba2+ + OH-=BaSO4↓+ H2O
D.硫酸铝溶液中加入过量的氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com