
| A. | 只有③④ | B. | 只有①② | C. | 只有①③⑤ | D. | 全部 |
分析 ①金属可以和酸反应生成对应的盐和氢气;
②非金属硅可以和强碱氢氧化钠反应生成硅酸钠和水;
③水溶液中电离出的阳离子全部是氢离子的化合物为酸,可以发生中和反应生成盐和水;
④水溶液中电离出阴离子全部是氢氧根离子的化合物为碱,可以发生中和反应生成盐和水;
⑤酸性氧化物是和碱反应生成盐和水的氧化物;
⑥碱性氧化物是和酸反应生成盐和水的氧化物.
解答 解:①金属的通性:可以和酸反应生成对应的盐和氢气,故①正确;
②非金属元素的单质硅可以和强碱氢氧化钠反应生成硅酸钠和氢气,故②正确;
③酸可以和碱发生中和反应生成盐和水,故③正确.
④碱可以和酸发生中和反应生成盐和水,故④正确;
⑤酸性氧化物是能和碱反应生成盐和水的化合物,故⑤正确;
⑥碱性氧化物是能和酸反应生成水的氧化物,故⑥正确;
故选D.
点评 本题考查了物质的性质知识,完成此题,可以依据教材知识进行,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 由元素X与Z形成的化合物中只含共价键 | |
| B. | XY2、ZY2、M2Y2的晶体分别属于3种不同类型的晶体 | |
| C. | 单质M的晶体是体心立方堆积,M的配位数是8 | |
| D. | X的氢化物X2H2分子中含有2个σ键和3个π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 c1<c2 | B. | c1>c2 | C. | c1=c2 | D. | 2 c1=c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Q2=Q1=92.4 | B. | Q2<Q1<92.4 | C. | Q1=Q2=92.4 | D. | Q1<Q2<92.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
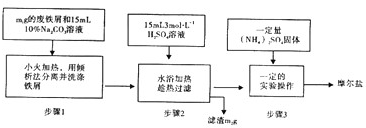
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com