
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2约45%,Fe2O3约40%,Al2O3约10%,MgO约5%。目前我国已经在技术上取得突破——从硫酸渣中分离出各种成分并加以利用。其流程和相关数据如下:
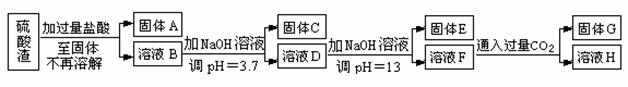
查资料得知:
| 物质名称 | 溶度积(Ksp) | pH值 | |
| 开始沉淀 | 完全沉淀 | ||
| Mg(OH)2 | 5.6×10-12 | 9.3 | 10.8 |
| Fe(OH)3 | 2.8×10-16 | 2.7 | 3.7 |
| Al(OH)3 | 1.3×10-33 | 3.7 | 4.7 |
请回答下列问题:
(1)写出固体A的化学式为 。
(2)若要测定溶液的pH是否达到3.7,下列实验用品中可选用的是 。
A.石蕊试液 B.广泛pH试纸 C.精密pH试纸 D.pH计
(3)完成下列离子反应方程式
①溶液D生成固体E ; ②溶液F生成固体G 。
(4)要将固体C、固体E和固体G都转化为相应的稳定氧化物,需进行的实验操作为 。
(5)若不考虑溶液体积的变化,请计算溶液H中c(Mg2+)= 。
科目:高中化学 来源: 题型:
下面是有关化学能和热能的叙述,其中正确的是( )
A.化学反应中不一定伴随着能量的变化
B.燃烧反应都可以看成物质内部的化学能转变为热能的放热反应
C.只要是加热才能发生的反应就一定是吸热反应
D.只要有能量变化的反应一定是化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 非金属元素R所形成的含氧酸盐(NaROb)中的R元素必定呈现正价
B. 只有非金属能形成含氧酸或含氧酸盐
C. 除稀有气体外的非金属元素都能生成不同价态的含氧酸
D.非金属的最高价含氧酸都具有强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)中和热的测定实验(如图)。
①量取反应物时,取50 mL 0.50 mol/L的盐酸,还应
加入的试剂是 (填序号)。
A.50 mL 0.50 mol/LNaOH溶液
B.50 mL 0. 55 mol/LNaOH溶液
C.1.0 g NaOH固体
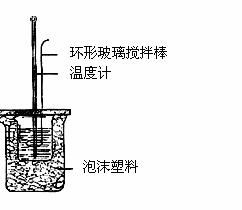
②在实验过程中,该同学需要测定并记录的实验数据有 (填序号)。
A.盐酸的浓度 B.盐酸的温度 C.氢氧化钠溶液的浓度
D.氢氧化钠溶液的温度 E.水的比热容 F.反应后混合溶液的最高温度
③若用50 mL 0.50 mol/L的醋酸溶液代替上述盐酸测定中和热,所得数据 (填“偏大”或“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法中不正确的是
A.KIO3+6HI=KI+3H2O+3I2 ,生成3mol I2转移电子的总数为5NA
B.标准状况下,5.6 L氧气中含有O的总数为0.5NA
C.25℃时,pH=13的Ba(OH)2溶液1.0L中含有OH-总数为0.1NA
D.20 g重水(D2O)中所含电子总数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
利用I2O5可消除CO污染或定量测定CO,反应为:
5CO(g)+I2O5(s)
 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g)
 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g)
 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
则ΔH 1= (用含ΔH 2和ΔH 3的代数式表示)。
 (2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如右图。请回答:
(2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如右图。请回答:
①从反应开始至a点时的反应速率为v(CO)= ,b点时化学平衡常数Kb= 。
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线。
③下列说法正确的是 。(填字母序号)
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的平均相对分子质量相等
C.增加I2O5的投料量有利于提高CO的转化率
D.b点和d点的化学平衡常数:Kb<Kd
(3)将500mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管,170℃下充分反应,用水—乙醇液充分溶解产物I2,定容到100mL。取25.00mL,用0.0100mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00mL,则样品气中CO的体积分数为 。(已知:气体样品中其他成分与I2O5不反应;2Na2S2O3+I2=2NaI+Na2S4O6)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验不能达到实验目的的是
A.用结晶法提纯混有少量氯化钾的硝酸钾
B.用KSCN检验溶液中Fe3+的存在
C.用湿润的淀粉碘化钾试纸检验氯气
D. 用酒精萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象.试判断下列哪组原子均可产生NMR现象( )
A.18O 31P B.元素周期表中ⅢA族所有元素的原子
C.19F 12C D.元素周期表中第三周期元素的所有原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com