
 ;
;分析 (1)乙烯与水在一定条件下发生加成反应生成乙醇;
(2)苯与浓硝酸在浓硫酸做催化剂、脱水剂条件下发生取代反应生成硝基苯和水;
(3)乙酸乙酯在烧碱溶液中水解生成醋酸钠和乙醇.
解答 解:(1)乙烯与水在一定条件下发生加成反应生成乙醇,化学方程式:CH2=CH2+H2O $\stackrel{一定条件下}{→}$ CH3CH2OH;
CH2=CH2+H2O $\stackrel{一定条件下}{→}$ CH3CH2OH;
(2)苯与浓硝酸在浓硫酸做催化剂、脱水剂条件下发生取代反应生成硝基苯和水,化学方程式 ;
;
故答案为: ;
;
(3)乙酸乙酯在烧碱溶液中的水解生成醋酸钠和乙醇,化学方程式:CH3COOC2H5+NaOH→CH3COONa+C2H5OH;
故答案为:CH3COOC2H5+NaOH→CH3COONa+C2H5OH.
点评 本题考查了化学方程式的书写,明确有机物结构特点是解题关键,注意反应发生的条件.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
| A. | 单质与氢气化合的难易程度:Z>L | |
| B. | Y的氧化物对应的水化物不能溶于过量的氨水 | |
| C. | Z单质在氧气中燃烧生成ZO3 | |
| D. | L、Q形成的简单离子核外电子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 运用化学反应原理研究溶液的组成与性质具有重要意义.请回答下列问题:
运用化学反应原理研究溶液的组成与性质具有重要意义.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥ | B. | ④⑤⑥ | C. | ①②⑤ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
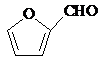 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$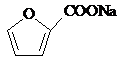 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.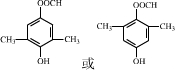 .
.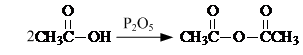 .
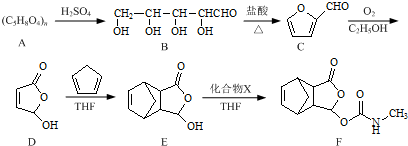
.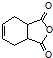 是合成抗病毒药阿昔洛韦的中间体,它可以用
是合成抗病毒药阿昔洛韦的中间体,它可以用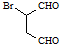 经氧化、消去、成酐一系列反应后再和原料M合成.
经氧化、消去、成酐一系列反应后再和原料M合成.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠(固体) | B. | 少量硫酸铜溶液 | C. | NaCl溶液 | D. | 加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com