
【题目】已知乙烯能发生以下转化: 
(1)乙烯的结构式为: .
(2)写出化合物官能团的化学式及名称:B中含官能团的化学式;官能团名称;
(3)写出反应的化学方程式②:反应类型:③:反应类型: .
科目:高中化学 来源: 题型:
【题目】为验证淀粉水解可生成还原性糖,进行了如下实验:①取少量淀粉加水制成溶液;②加热煮沸;③加入新制的氢氧化铜悬浊液;④加入几滴稀硫酸;⑤再加热;⑥加入碱液中和并使溶液呈碱性。正确的操作排列顺序是
A.①④⑤⑥③②B.⑤④③②①⑥C.①④②⑥③⑤D.①⑤③④⑥②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,而辛是由C元素形成的单质.已知:甲+乙=丁+辛,甲+丙=戊+辛;常温下0.1mol/L丁溶液的pH为13,则下列说法正确的是( )
A.元素C形成的单质可以在点燃条件分别与元素A、B、D形成的单质化合,所得化合物均存在共价键
B.元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B)
C.1.0 L 0.1 mol/L戊溶液中含阴离子总的物质的量小于0.1 mol
D.1 mol甲与足量的乙完全反应共转移约1.204×1024个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素性质呈周期性变化的原因是( )
A. 相对原子质量逐渐增大B. 核电荷数逐渐增大
C. 核外电子排布呈周期性变化D. 元素的化合价呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是( )
A.向稀HNO3中滴加Na2SO3溶液SO ![]() +2H+═SO2↑+H2O
+2H+═SO2↑+H2O
B.CuSO4溶液与H2S反应的离子方程式:Cu2++S2﹣═CuS↓
C.氯气溶于水:Cl2+H2═2H++Cl﹣+ClO﹣
D.向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2═4Na++2Cu(OH)2↓+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁是海水中含量较多的金属元素,单质镁、镁合金以及镁的化合物在科学研究和工业生产中用途非常广泛.
(1)Mg2Ni是一种储氢合金,已知:
Mg(s)+H2(g)=MgH2(s)△H1=﹣74.5kJmol﹣1
Mg2Ni(s)+2H2(g)=Mg2NiH4(s)△H2=﹣64.4kJmol﹣1
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)△H3
则△H3=kJmol﹣1
(2)工业上可用电解熔融的无水氯化镁获得镁.其中氯化镁晶体脱水是关键的工艺之一.一种正在试验的氯化镁晶体脱水的方法是:先将MgCl26H2O转化为MgCl2NH4ClnNH3 , 然后在700℃脱氨得到无水氯化镁,脱氨反应的化学方程式为;
(3)镁的一种化合物氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等.为了确定实验室制备的Mg(ClO3)26H2O的纯度,做如下试验:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10mL于锥形瓶中,加入10mL稀硫酸和20mL 1.000molL﹣1的FeSO4溶液,微热.
步骤3:冷却至室温,用0.100molL﹣1 K2Cr2O7溶液滴定至终点,此过程中反应的离子方程式为:Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O.
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00mL.产品中Mg(ClO3)26H2O的纯度为(用百分号表示,精确到小数点后一位)
(4)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率如1图所示.250~300℃时,温度升高而乙酸的生成速率降低的原因是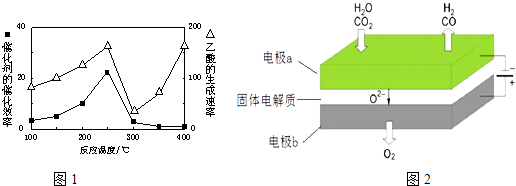
(5)Li2O、Na2O、MgO均能吸收CO2 .
①如果寻找吸收CO2的其它物质,下列建议合理的是
a.可在碱性氧化物中寻找
b.可在ⅠA、ⅡA族元素形成的氧化物中寻找
c.可在具有强氧化性的物质中寻找
②Li2O吸收CO2后,产物用于合成Li4SiO4 , Li4SiO4用于吸收、释放CO2 , 原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2 , Li4SiO4再生,说明该原理的化学方程式是
(6)利用反应A可将释放的CO2转化为具有工业利用价值的产品.反应A:CO2+H2O ![]() CO+H2+O2高温电解技术能高效实现(3)中反应A,工作原理示意图如图2:CO2在电极a放电的反应式是 .
CO+H2+O2高温电解技术能高效实现(3)中反应A,工作原理示意图如图2:CO2在电极a放电的反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释物质用途或现象的反应方程式不正确的是( )
A.汽车尾气中发生的催化转化反应:2NO+2CO ![]() N2+2CO2
N2+2CO2
B.铝热反应用于焊接钢轨:2Al+Fe2O3 ![]() Al2O3+2Fe
Al2O3+2Fe
C.燃煤时加入石灰石减少SO2排放:2CaCO3+2SO2+O2 ![]() 2CaSO3+2CO2
2CaSO3+2CO2
D.用Na2CO3溶液处理水垢中的不溶物CaSO4:CaSO4+CO![]() ═CaCO3+SO
═CaCO3+SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 2L 容积不变的密闭容器内,800℃时反应 2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如下表:
t/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)用O2的反应速率表示 0~2s 内该反应的平均反应速率 v= . 若上述反应在850℃下进行,反应2s时 n(NO)=0.009mol,并且不再随时间而改变,则该反应是热反应.
(2)图中表示NO2浓度变化的曲线是(填字母). 
(3)能说明该反应已达到平衡状态的是(填序号).
A.v(NO2)=2v(O2)
B.容器内的压强保持不变
C.v逆(NO)=2v正(O2)
D.容器内气体密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是(填序号).
A.及时分离出NO2
B.适当升高温度
C.增大O2的浓度
D.选择高效催化剂.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com