
【题目】过氧硫酸氢钾复合盐(K2SO4KHSO42KHSO5)易分解,可用作漂白剂、NOx和SO2等的脱除剂。某研究小组制备过氧硫酸氢钾复合盐的流程如图所示。

已知:浓硫酸与H2O2反应,部分转化为过硫酸(化学式为H2SO5,是一种一元强酸)
(1)H2SO5中硫元素的化合价为+6价,其中过氧键的数目为________;工业上用过氧硫酸氢钾复合盐溶液脱除NO时,反应的离子方程式为___________________________。
(2)若反应物的量一定,在上述流程的“转化”步骤中需用冰水浴冷却,且缓慢加入浓硫酸,其目的是___________________________。
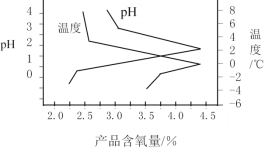
(3)“结晶”操作中,加入K2CO3即可获得过氧硫酸氢钾复合盐晶体,该过程的化学方程式为______________________________。过氧硫酸氢钾复合盐产率(以产品含氧量表示)随溶液pH和温度的变化关系如图所示,则该过程适宜的条件是_________________。
(4)产品中KHSO5含量的测定:取1.000g产品于锥形瓶中,用适量蒸馏水溶解,加入5mL5%的硫酸和5mL25%的KI溶液,再加入1mL淀粉溶液作指示剂,用0.2000mol·L-1硫代硫酸钠标准液滴定至终点,消耗标准液的体积为25.00mL。
已知:2KHSO5+4KI+H2SO4 = 2I2+3K2SO4+2H2O I2+2Na2S2O3 =Na2S4O6+2NaI
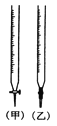
①用_____滴定管盛装标准浓度的硫代硫酸钠溶液(填“甲”或“乙”)。
②产品中KHSO5的质量分数为___________。
【答案】1 3HSO5-+2NO+H2O = 3SO42-+2NO3-+5H+ 防止浓硫酸与H2O2溶液混合时放出大量热使H2O2分解 5K2CO3+4H2SO5+4H2SO4 =2(K2SO4KHSO42KHSO5)↓+5CO2↑+5H2O 控制pH在2.0~2.5之间,温度在0℃左右 乙 38.00%
【解析】
(1)H2SO5中硫元素的化合价为+6价,依据化合价的代数和为0计算,有2个氧原子显-1价,所以过氧键的数目为1。答案为1;
工业上用过氧硫酸氢钾复合盐溶液脱除NO时,反应的离子方程式为3HSO5-+2NO+H2O = 3SO42-+2NO3-+5H+。答案为3HSO5-+2NO+H2O = 3SO42-+2NO3-+5H+
(2)在“转化”步骤中,30%的H2O2溶液加入98%的浓硫酸中,相当于浓硫酸稀释,会放出大量的热,而H2O2受热易分解,所以需用冰水浴冷却,且缓慢加入浓硫酸。
答案为:防止浓硫酸与H2O2溶液混合时放出大量热使H2O2分解;
(3)“结晶”操作中,加入K2CO3即可获得过氧硫酸氢钾复合盐晶体,该过程的化学方程式为5K2CO3+4H2SO5+4H2SO4 =2(K2SO4KHSO42KHSO5)↓+5CO2↑+5H2O。
答案为:5K2CO3+4H2SO5+4H2SO4 =2(K2SO4KHSO42KHSO5)↓+5CO2↑+5H2O
从溶液pH看,过氧硫酸氢钾复合盐产率在2.0~2.5之间时最大;从温度看,过氧硫酸氢钾复合盐产率在0℃左右最大,所以该过程适宜的条件是控制pH在2.0~2.5之间,温度在0℃左右。答案为:控制pH在2.0~2.5之间,温度在0℃左右;
(4) ① 硫代硫酸钠溶液呈碱性,应放在碱式滴定管内。答案为乙;
② 由反应2KHSO5+4KI+H2SO4 = 2I2+3K2SO4+2H2O和I2+2Na2S2O3 =Na2S4O6+2NaI可得出如下关系式:KHSO5——2Na2S2O3
n(Na2S2O3)=0.2mol/L×0.025L=0.005mol,n(KHSO5)=0.0025mol
产品中KHSO5的质量分数为:![]()
答案为:38.00%。


科目:高中化学 来源: 题型:
【题目】商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1000℃左右冶炼,可能涉及的反应有:
①Cu2(OH)2CO3![]() 2CuO+CO2↑+H2O;
2CuO+CO2↑+H2O;
②2CuO+C![]() 2Cu+CO2↑;
2Cu+CO2↑;
③CuO+CO![]() Cu+CO2;
Cu+CO2;
④CO2+C![]() 2CO。
2CO。
(1)从四种基本反应类型来看,①②④的反应类型分别为①___________,②___________,④___________。
(2)反应③中,____________发生氧化反应,__________发生还原反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X中可能含有Na+、Fe3+、Mg2+、HCO3-、Cl-、SO42-、SO32-中的若干种,所含离子的物质的量浓度均相同,为了确定该溶液的组成,某同学取100mL上述溶液X,进行如下实验:
![]()
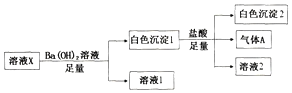
下列说法正确的是
A. 气体A可能是CO2或SO2
B. 溶液X中一定存在Na+、Mg2+、HCO3-、SO42-
C. 溶液X中一定不存在Fe3+和Mg2+,可能存在-Na+
D. 分别在溶液1和溶液2中加入硝酸酸化的硝酸银溶液都能生成白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列有机物的系统命名不正确的是:
A. CH2=CHCH2CH3 1—丁烯
B. C(CH3)4 2,2—二甲基丙烷
C. CH3C≡CCH2CH3 2—戊炔
D. ![]() 对二甲苯
对二甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,HNO2和CH3COOH的电离常数分别为5.0×10-4和1.7×10-5。将pH相同、体积均为V0的两种酸溶液分别加水稀释至体积V,pH随![]() 的变化如图所示,下列叙述错误的是
的变化如图所示,下列叙述错误的是
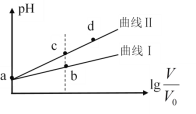
A.曲线Ⅰ代表CH3COOH溶液
B.溶液中水的电离程度:b点小于c点
C.相同体积a点的两种酸分别与NaOH溶液恰好中和后,溶液中n(NO2-)>n(CH3COO-)
D.由c点到d点,溶液中![]() 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
保持不变(其中HA、A-分别代表相应的酸和酸根离子)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法不正确的是( )
)是最简单的一种。下列关于该化合物的说法不正确的是( )
A.与环戊烯互为同分异构体
B.二氯代物超过两种
C.所有碳原子均处同一平面
D.1mol螺[2,2]戊烷充分燃烧需要7molO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,气体被还原的是
A.水蒸气使 CuSO4固体变蓝B.氯气使浅绿色 FeC12 溶液变黄
C.H2使灼热CuO 固体变红D.氨气使A1Cl3溶液产生白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用碳酸钠晶体配制1.00mol/L的Na2CO3溶液100mL,造成所配溶液浓度偏高的原因是( )
A. 烧杯和玻璃棒没有洗涤
B. 向容量瓶转移液体时,容量瓶事先用蒸馏水洗涤
C. 定容时俯视刻度线
D. 称量碳酸钠晶体(Na2CO310H2O)的烧杯未干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】被誉为“矿石熊猫”的香花石,由我国地质学家首次发现,它由前20号元素中的6种主族元素组成,其化学式为Y2X3(ZWR4)3T2,其中X、Y、Z为金属元素,Z的最外层电子数与次外层电子数相等,X、Z位于同族,Y、Z、R、T位于同周期,R最外层电子数是次外层的3倍,T无正价,X与R原子序数之和是W的2倍。下列说法错误的是( )
A.原子半径:Y>Z>R>TB.XR2、WR2两种化合物中R的化合价相同
C.最高价氧化物对应的水化物的碱性:X>ZD.气态氢化物的稳定性:W<R<T
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com