
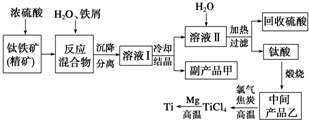
 金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图:
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中.“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如图:
| ||
| ||
| ||
| ||
| ||
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、100mL 0.5mol/L KClO3溶液 |
| B、200mL 2.5mol/L MgCl2溶液 |
| C、300mL 2mol/L AlCl3溶液 |
| D、400mL1mol/L 盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入合金的质量可能为3.2g |
| B、参加反应的硝酸的物质的量为0.4mol |
| C、沉淀完全时消耗NaOH的物质的量为0.3mol |
| D、还原产物的体积范围2.24L<V还原产物<6.72L |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、0.5 mol?L-1 |
| B、0.1 mol?L-1 |
| C、1 mol?L-1 |
| D、1.5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
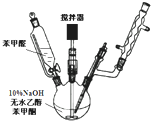 (1)制备过程中(如图),需在搅拌下滴加苯甲醛,并控制滴加速度使 反应温度维持在25~30℃,说明该反应是
(1)制备过程中(如图),需在搅拌下滴加苯甲醛,并控制滴加速度使 反应温度维持在25~30℃,说明该反应是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 准确称取氯化钾固体,放入到100mL的容量瓶中,加水溶解,振荡摇匀,定容 | 配制100mL一定浓度的氯化钾溶液 |
| B | 下层液体从分液漏斗下端口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 | 取出分液漏斗中所需的上层液体 |
| C | 向盛有沸水的烧杯中滴加FeCl3饱和溶液继续加热至溶液呈红褐色 | 制备Fe(OH)3胶体 |
| D | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支试管加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com