
| A. | 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的$\frac{2}{3}$,液体也不能蒸干 | |
| B. | 可用稀硝酸鉴别MgI2、AgNO3、Na2CO3、NaAlO2四种溶液 | |
| C. | 将Mg(OH)2沉淀转入烧杯中,加足量稀硫酸溶解,加热浓缩、冷却结晶、过滤后得到晶体 | |
| D. | 除去乙酸乙酯中的乙酸杂质:加入氢氧化钠溶液,分液 |
分析 A.蒸馏时液体不能过多,且不能蒸干液体;
B.MgI2、AgNO3、Na2CO3、NaAlO2分别与硝酸反应的现象为:紫色溶液、无现象、无色气体、先生成白色沉淀后消失;
C.Mg(OH)2与稀硫酸反应生成硫酸镁,蒸发浓缩、冷却结晶析出晶体;
D.二者均与NaOH反应.
解答 解:A.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的$\frac{2}{3}$,防止溢出,且不能蒸干液体,操作合理,故A正确;
B.MgI2、AgNO3、Na2CO3、NaAlO2分别与硝酸反应的现象为:紫色溶液、无现象、无色气体、先生成白色沉淀后消失,现象不同,可鉴别,故B正确;
C.Mg(OH)2与稀硫酸反应生成硫酸镁,蒸发浓缩、冷却结晶析出晶体,过滤后得到晶体,故C正确;
D.二者均与NaOH反应,不能除杂,应选饱和碳酸钠溶液、分液除杂,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、物质的鉴别、混合物分离提纯、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 9.6×10-3 | B. | 4.8×10-5 | C. | 1.25×10-6 | D. | 2.0×10-4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 环境要求 | 离子组 |
| A | Fe2(SO4)3溶液中 | K+、AlO2-、Cl-、NO3- |
| B | 与Al反应能放出H2的溶液中 | Fe2+、Na+、NO3-、SO42- |
| C | 水电离产生的c(H+)=10-12mol/L的溶液 | ClO-、CO32-、NH4+、NO3-、SO32- |
| D | 向溶液中逐滴滴加烧碱溶液先有沉淀产生,后沉淀消失 | Na+、Al3+、Cl-、SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 漂白粉 | 硫酸 | 醋酸 | 干冰 |
| B | 氢氧化钡 | 蔗糖溶液 | 硫酸钡 | 溴水 | 二氧化硫 |
| C | 胆矾 | 石灰水 | 氧化铝 | 水 | 氯气 |
| D | 小苏打 | 氢氧化铁胶体 | 氯化银 | 次氯酸 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入NaOH溶液:Cl2+OH-=Cl-+ClO-+H2O | |
| B. | NaHCO3溶液中加入稀HCl:CO32-+2H+=CO2↑+H2O | |
| C. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | Cu溶于稀HNO3:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1L、1mol/L NaCl溶液中取出10mLNaCl溶液,其浓度仍为1mol/L | |
| B. | 配制0.5L、10mol/L的盐酸,需要氯化氢气体112升(标况) | |
| C. | 0.5L、2mol/L BaCl2溶液中Ba2+ 和 Cl-的总个数约为3×6.02×1023 | |
| D. | 10g、98%的浓硫酸(密度为1.84g/cm3 )与10mL、1.84mol/L的浓硫酸浓度不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
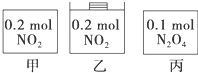 甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )
甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡.下列说法正确的( )| A. | 平衡时各容器内n(NO2)的大小顺序为乙>甲>丙 | |
| B. | 平衡时NO2的百分含量:乙>甲=丙 | |
| C. | 平衡时甲中NO2与丙中N2O4的转化率一定相同 | |
| D. | 平衡时混合物的平均相对分子质量:乙>甲=丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
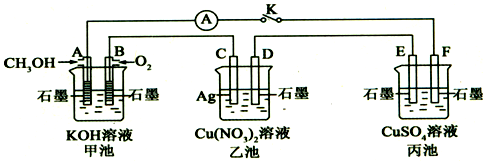
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2SO2(g)+O2(g)?2SO3(g)△H=-196kJ/mol(反应热) | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ/mol(燃烧热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=-116.2kJ/mol(反应热) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com