
| A、将碘水倒入分液漏斗,加适量四氯化碳,振荡后静置,可将碘萃取到下层液体中 |
| B、向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失 |
| C、加入盐酸以除去硫酸钠中的少量碳酸钠杂质 |
| D、在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,会得到含氢氧化铁的FeCl3溶液 |


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
 的质量分数,在实验室中按以下步骤进行实验:
的质量分数,在实验室中按以下步骤进行实验:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中氧化剂与还原剂的物质的量比值为3:2 |
| B、反应中NaOH既不是氧化剂也不是还原剂 |
| C、当有0.2mol Fe(OH)3参加反应时转移的电子数目为1.204×1023 |
| D、反应中NaClO被还原,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸银溶液存放在无色试剂瓶中 |
| B、金属钠保存在CCl4中(钠的密度小于CCl4) |
C、 浓硫酸的装运包装箱应贴上如图所示的标识 |
| D、氢氧化钠溶液保存在带玻璃塞的玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在测定硫酸铜晶体结晶水含量的实验中,最少称量4次 |
| B、使用pH试纸测定溶液的pH时,首先用蒸馏水润湿pH试纸的做法是错误的,测定的结果也一定是错误的 |
| C、配制一定物质的量浓度额溶液,容量瓶内有蒸馏水对配制结果无影响 |
| D、酸碱中和滴定时,锥形瓶内有蒸馏水对滴定结果无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水,将湿润的红色石蕊试纸放在试管口 |
| B、加NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口 |
| C、加NaOH溶液,加热,滴入酚酞试剂 |
| D、加NaOH溶液,加热,滴入紫色石蕊试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
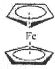 )是一种典型的金属有机化合物,实验室常用新制氯化亚铁和环戊二烯在碱性条件下反应得到.反应原理为FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O.二茂铁的熔点为172~173℃,在100℃开始升华.能溶于乙醚、二甲亚砜等溶剂,不溶于水,对碱和非氧化性酸稳定.某研究小组设计的实验方案和制备装置示意图如下:
)是一种典型的金属有机化合物,实验室常用新制氯化亚铁和环戊二烯在碱性条件下反应得到.反应原理为FeCl2+2C5H6+2KOH→Fe(C5H5)2+2KCl+2H2O.二茂铁的熔点为172~173℃,在100℃开始升华.能溶于乙醚、二甲亚砜等溶剂,不溶于水,对碱和非氧化性酸稳定.某研究小组设计的实验方案和制备装置示意图如下: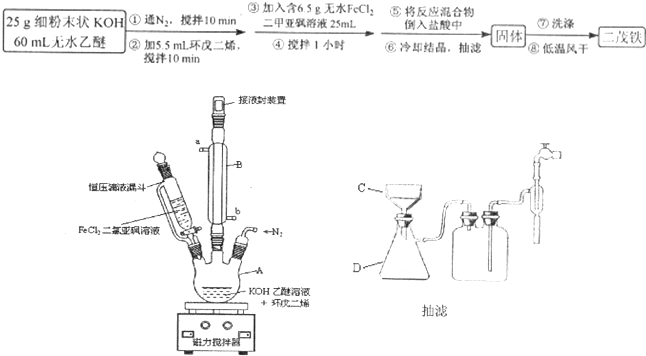
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、60% | B、40% |
| C、24% | D、4% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com