
分析 (1)该反应为气体体积不变的反应,恒温恒容条件下,若加入1molH2,1molBr2平衡时HBr的物质的量为n,则上述配比转化到一边即n(H2)=1mol,n(Br2)=1mol,则与原平衡完全等效,在平衡时HBr的物质的量仍为n;则上述配比转化到一边满足H2与Br2物质的量之比为1:1,则与原平衡成比例等效,则HBr体积分数为a%,据此判断;
(2)该反应为气体体积不变的反应,恒温恒压条件下,若加入1molH2,1molBr2平衡时HBr的物质的量为n,则上述配比转化到一边即n(H2)=1mol,n(Br2)=1mol,则与原平衡完全等效,在平衡时HBr的物质的量仍为n;则上述配比转化到一边满足H2与Br2物质的量之比为1:1,则与原平衡成比例等效,则HBr体积分数为a%,据此判断;
解答 解:(1)该反应为气体体积不变的反应,恒温恒容条件下,若加入1molH2,1molBr2平衡时HBr的物质的量为n,则上述配比转化到一边即n(H2)=1mol,n(Br2)=1mol,则与原平衡完全等效,在平衡时HBr的物质的量仍为n;则上述配比转化到一边满足H2与Br2物质的量之比为1:1,则与原平衡成比例等效,则HBr体积分数为a%,
①1molH2 1molHBr 转化到一边得n(H2)=1.5mol,n(Br2)=0.5mol,与原平衡不等效;
②2molHBr转化到一边得n(H2)=1mol,n(Br2)=1mol,与原平衡完全等效,所以平衡时HBr的物质的量仍为n,HBr体积分数仍为a%;
③0.5molH2,0.5molBr21molHBr转化到一边得n(H2)=1mol,n(Br2)=1mol,与原平衡完全等效,所以平衡时HBr的物质的量仍为n,HBr体积分数仍为a%;
④1molH2,1molBr2 2molHBr转化到一边得n(H2)=2mol,n(Br2)=2mol,与原平衡成比例等效,所以平衡时HBr的物质的量为2n,HBr体积分数仍为a%;
所以平衡时HBr的物质的量仍为n的是②③;若HBr体积分数为a%,则上述配比在平衡时仍为a%的是②③④,故答案为:②③;②③④;
(2)该反应为气体体积不变的反应,恒温恒压条件下,若加入1molH2,1molBr2平衡时HBr的物质的量为n,则上述配比转化到一边即n(H2)=1mol,n(Br2)=1mol,则与原平衡完全等效,在平衡时HBr的物质的量仍为n;则上述配比转化到一边满足H2与Br2物质的量之比为1:1,则与原平衡成比例等效,则HBr体积分数为a%,
①1molH2 1molHBr 转化到一边得n(H2)=1.5mol,n(Br2)=0.5mol,与原平衡不等效;
②2molHBr转化到一边得n(H2)=1mol,n(Br2)=1mol,与原平衡完全等效,所以平衡时HBr的物质的量仍为n,HBr体积分数仍为a%;
③0.5molH2,0.5molBr21molHBr转化到一边得n(H2)=1mol,n(Br2)=1mol,与原平衡完全等效,所以平衡时HBr的物质的量仍为n,HBr体积分数仍为a%;
④1molH2,1molBr2 2molHBr转化到一边得n(H2)=2mol,n(Br2)=2mol,与原平衡成比例等效,所以平衡时HBr的物质的量为2n,HBr体积分数仍为a%;
所以平衡时HBr的物质的量仍为n的是②③;若HBr体积分数为a%,则上述配比在平衡时仍为a%的是②③④,故答案为:②③;②③④;
点评 本题考查的是等效平衡及化学平衡的有关计算,采用极限反应法是解题的关键,难度较大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 正盐 | 酸式盐 |
| CO2 | Na2O | H2CO3 | NaOH | Na2CO3 | NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮气分子的结构式:N-N | B. | Mg2+的结构示意图: | ||
| C. | 乙醇的结构简式:CH3CH2OH | D. | 二氧化碳电子: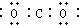 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,等体积的水和CO2,含有的氧原子数目为1:2 | |
| B. | 含有NA个阴离子的Na2O2与足量水反应,转移电子数为2NA | |
| C. | 向含有1molFeI2的溶液中通入适量氯气,当有NA个Fe2+被氧化时,共转移电子数为3NA | |
| D. | 一个NO分子质量为a g,一个NO2分子质量是b g,则NA个O2的质量为(b-a)NAg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④③ | B. | ②③⑤③ | C. | ①③④③ | D. | ②⑤③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com