
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.![]()
B. Al![]() NaAlO2
NaAlO2![]() Al(OH)3
Al(OH)3
C. Fe![]() FeCl2
FeCl2![]() FeCl3
FeCl3
D. Na![]() Na2O
Na2O![]() NaOH
NaOH
科目:高中化学 来源: 题型:
【题目】向含有0.01 mol Cu,a mol Cu2O、b mol CuO的混合物中滴加6 mol·L-1的稀硝酸溶液至10ml时,固体恰好完全溶解,得到标准状况下224mL气体(纯净物)。下列说法正确的是
A.反应过程中转移0.01 mol电子B.a:b=1:1
C.被还原的硝酸为0.06 molD.将少量铁粉投入该稀硝酸中能生成Fe(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题(Cl2易溶于CCl4)。
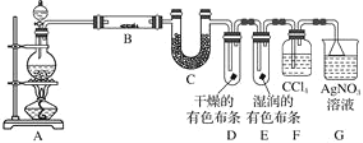
(1)若用含有7.3 g HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2质量总是小于3.55 g的原因是________________________________。
(2)①装置B中盛放的试剂名称为________________,作用是________________________________,现象是_____________________________。
②装置D和E中出现的不同现象说明的问题是___________________。
③装置F的作用是__________________________________________。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在________与________之间(填装置字母序号),装置中应放入________(填写试剂或用品名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。上述物质有如图转化关系:下列说法正确的是( )
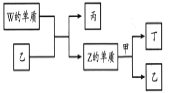
A.甲、乙、丙中沸点最高的是甲
B.甲常用作制冷剂
C.四种元素形成的单质中W的氧化性最弱
D.四种元素原子半径大小:W > Z > Y > X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知氢有3种常见原子:11H、21H、31H(或H、D、T),氯有2种常见核素原子:35Cl、37Cl,氯气与氢气形成的氯化氢分子的相对分子质量有________种。
(2)质量相同的H216O和D216O所含质子数之比为______,中子数之比为________,电解产生的氢气在同温同压下体积之比为________,质量之比为________。
(3)2 g AO32-电子数比质子数多3.01×1022个,则A的相对原子质量为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组用如图所示装置进行实验,探究铁和浓硫酸反应的产物及性质。(夹持装置已略,气密性已检验)
实验开始前,先打开活塞K通一段时间N2。关闭活塞K后,向A中滴加一定量的浓硫酸,加热观察到A中铁片上有气泡产生。
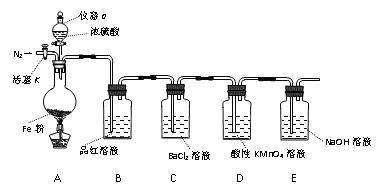
请回答下列问题:
(1)仪器a的名称是____。实验开始前,先通一段时间N2的目的是____。
(2)加热一段时间后发现B装置中溶液褪色,说明有____(填化学式)生成。再取出A中反应后的溶液少许,加入KSCN溶液未出现血红色,浓硫酸与铁反应的化学方程式是____。
(3)C装置中____(填“有”或“无”)沉淀生成。D中溶液紫色褪去,体现气体产物的____性(填“氧化”、“还原”或“漂白性”)。
(4)E装置的作用是____。(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质结构与性质)
钴及其化合物在生产中有重要作用,回答下列问题
(1)钴元素基态原子的电子排布式为________________,未成对电子数为________________。
(2)配合物[Co(NH3)4(H2O)2]Cl3是钴重要化合物
①H2O的沸点___ (填“高于”或“低于”)H2S,原因是_______;H2O中O的杂化形式为_____。H2O是_____分子(填“极性”或“非极性”)。
②[Co(NH3)4(H2O)2]Cl3中的Co3+配位数为___。阳离子的立体构型是___________。[Co(NH3)4(H2O)2]Cl3若其中有两个NH3分子被Cl取代,所形成的[Co(NH3)2Cl2(H2O)2]3+的几何异构体种数有(不考虑光学异构)___________种。
(3)一氧化钴的晶胞如图,则在每个Co2+的周围与它最接近的且距离相等的Co2+共有_____个,若晶体中Co2+与O2-的最小距离为acm,则CoO的晶体密度为_______(用含NA和a的代数式表示。结果g/cm3,已知:M(Co)=59g/mol;M(O)=16g/mol,设阿伏加德罗常数为NA)。
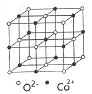
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铝镁[MgaAlb(OH)c(CO3)d]在一定条件下的转化如下图所示,下列说法正确的是
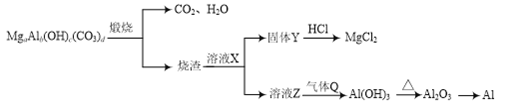
A. a、b、c、d符合关系式:2a+3b=c+2d
B. X可能为NaOH
C. Q可能为NH3
D. 工业上用CO还原Al2O3的方法制取金属Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】顺式乌头酸是一种重要的食用增味剂,其结构如下图所示。下列说法正确的是
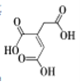
A.该有机物的分子式为:C6H8O6
B.该有机物只含有一种官能团
C.该有机物能使酸性KMnO4溶液、溴的四氯化碳溶液褪色,且原理相同
D.等物质的量的顺式乌头酸分别与足量的NaHCO3和Na反应,产生相同条件下的气体体积之比为2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com