
| A. | 水泥 | B. | 木材 | C. | 陶瓷 | D. | 铝合金 |
分析 高分子化合物(又称高聚物)一般相对分子质量高于10000,结构中有重复的结构单元;有机高分子化合物可以分为天然有机高分子化合物(如淀粉、纤维素、蛋白质天然橡胶等)和合成有机高分子化合物(如聚乙烯、聚氯乙烯等),据此即可解答.
解答 解:A.水泥的主要成分为:硅酸三钙3CaO•SiO2,硅酸二钙2CaO•SiO2,铝酸三钙3CaO•Al2O3,属于硅酸盐,故A错误;
B.木材是纤维素,化学式为:(C6H10O5)n,相对分子质量在一万以上,为天然高分子化合物,故B正确;
C.陶瓷主要成分硅酸盐,属于无机非金属材料,故C错误;
D.铝合金是以铝为主的合金,属于无机金属材料,故D错误;
故选B.
点评 本题考查了天然高分子化合物判别,注意式量的大小和天然是解题的关键,平时须注意相关物质的成分、分类,题目难度较小.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 蚊虫叮咬处涂抹肥皂水可止痛痒 | |
| B. | 大力实施矿物燃料脱硫脱硝技术,能减少硫、氮氧化物的排放 | |
| C. | 明矾净水时发生了化学及物理变化,能起到净水作用,而没有杀菌、消毒的作用 | |
| D. | 铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
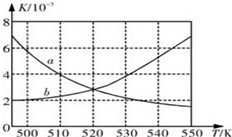
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/(kJ•mol-1) | 738 | 1451 | 7733 | 10 540 | 13 630 |
| 离子晶体 | NaCl | KC1 | CaO |
| 晶格能/(kJ•mol-1) | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1molN2和3molH2混合发生反应,转移的电子总数为6NA | |
| B. | 1L0.1mol•L-1的Na2CO3溶液中阴离子的总数大于0.1NA | |
| C. | 向FeI2溶液中通入适量Cl2,当有2molFe2+被氧化时,消耗Cl2的分子数为NA | |
| D. | 1mol-CH3中所含的电子总数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
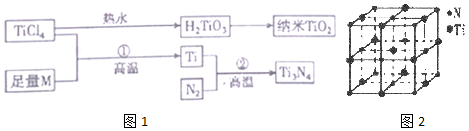
 Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)
Ⅰ:为了减少CO的排放,某环境研究小组以CO和H2 为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g)| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | - |
| n(CO)/mol | 1.0 | - | 0.425 | 0.2 | 0.2 |
| n(CH3OCH3)/mol | 0 | 0.15 | - | - | 0.4 |
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
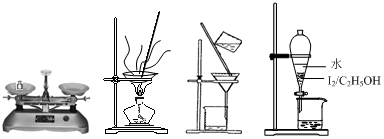
| A. | 称量 | B. | 灼烧 | C. | 过滤 | D. | 萃取 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
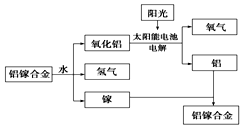 美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )
美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示).下列有关该工艺的说法错误的是( )| A. | 铝镓合金与水反应的化学方程式为2Al+3H2O$\frac{\underline{\;一定条件\;}}{\;}$Al2O3+3H2↑ | |
| B. | 总反应式为2H2O$\frac{\underline{\;一定条件\;}}{\;}$2H2↑+O2↑ | |
| C. | 该过程中,能量的转化形式只有两种 | |
| D. | 铝镓合金可以循环使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热、通氢气、停止加热、继续通氢气至试管冷却 | |
| B. | 通氢气、加热、停止加热、继续通氢气至试管冷却 | |
| C. | 通氢气后立即点燃酒精灯加热 | |
| D. | 停止加热后立即停止通氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
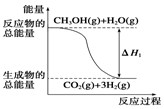 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:| A. | 1 mol CH3OH完全燃烧放出192.9 kJ热量 | |
| B. | 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程不一定要吸收能量 | |
| D. | 根据②推知:CH3OH(1)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H<-192.9 kJ•mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com