
【题目】(1)工业上用112 L(标准状况)氯气与足量石灰乳反应,制得的漂白粉中有效成分Ca(ClO)2的最大含量为___________mol。
(2)向一定量石灰乳中缓慢通入氯气,随着反应的进行,温度升高,开始产生Ca(ClO3)2。体系中ClO-和ClO3-的物质的量(n)与反应时间(t)的关系曲线如图1所示(不考虑氯气和水的反应)。
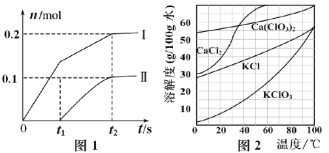
①t2时刻后,溶液中ClO-和ClO3-的物质的量之比为_____________。
②该反应过程中消耗Ca(OH)2的质量为_____________。
(3)向Ca(ClO3)2浓溶液中加入稍过量的KCl固体可转化为KClO3,如图2,从该溶液中分离出KClO3固体的实验方法是________________(不要求填具体操作步骤)。
【答案】2.5 2:1 37g 冷却结晶法或降温结晶法
【解析】
(1)根据方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O进行计算;
(2)当温度低时,氯气和氢氧化钙反应生成氯化钙和次氯酸钙;当温度高时,生成氯酸钙和氯化钙,刚开始反应时,温度较低,氯气和氢氧化钙反应生成氯化钙和次氯酸钙,所以图1中曲线I表示离子ClO-的物质的量随反应时间变化的关系,图中曲线Ⅱ表示ClO3-的物质的量随反应时间变化的关系;据图像及氧化还原反应中得失电子数相等进行分析和计算;
(3)从图2看出KClO3溶解度受温度影响比较大,可用冷却热饱和溶液的方法,从溶液中分离出KClO3固体。
(1)n(Cl2)= ![]() =5mol,根据方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,n(Ca(ClO)2)=
=5mol,根据方程式:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,n(Ca(ClO)2)=![]() =2.5mol;
=2.5mol;
(2)当温度低时,氯气和氢氧化钙反应生成氯化钙和次氯酸钙;当温度高时,生成氯酸钙和氯化钙,刚开始反应时,温度较低,氯气和氢氧化钙反应生成氯化钙和次氯酸钙,所以图1中曲线I表示离子ClO-的物质的量随反应时间变化的关系,图中曲线Ⅱ表示ClO3-的物质的量随反应时间变化的关系;
①t2时刻后,溶液中ClO-和ClO3-的物质的量之比为0.2:0.1=2:1;
②根据氧化还原反应中得失电子数相等计算Cl-的物质的量,设被还原的氯离子的物质的量为n,则n×1=0.20mol×1+0.1mol×5=0.70mol,含氯离子的物质的量为:0.70mol+0.2mol+0.1mol=1.0mol,氯化钙、次氯酸钙、氯酸钙中钙离子和含氯离子的个数比为1:2,所以所取石灰乳中含有Ca(OH)2的物质的量为0.5mol,质量为0.5mol×74g·mol-1=37g;
(3)向Ca(ClO3)2浓溶液中加入稍过量的KCl固体可转化为KClO3,从图2看出KClO3溶解度受温度影响比较大,可用冷却热饱和溶液的方法,从溶液中分离出KClO3固体,即:冷却结晶法或降温结晶法。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】一种肼燃料电池的结构如图所示,下列说法正确的是( )
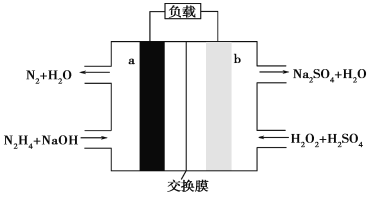
A. a极是正极,电极反应式为N2H4-4e-+4OH-=N2↑+4H2O
B. 电路中每转移NA个电子,就有1mol Na+穿过膜向正极移动
C. b极的电极反应式为H2O2+2e-=2OH-
D. 用该电池作电源电解饱和食盐水,当得到0.1mol Cl2时,至少要消耗0.1mol N2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.海藻中提取碘的流程如图,已知②中发生反应的化学方程式为:Cl2+2KI=2KCl+I2。请 回答下列问题:
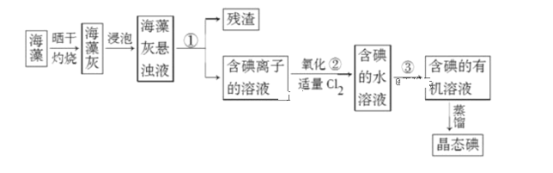
(1)指出提取碘的过程中有关实验操作①和③的名称:________;________。
(2)在 3 mL 碘水中,加入 1 mL 四氯化碳,振荡、静置后,观察到试管里的分层现象是下图中的________ (注:试管中深色区为紫红色溶液)。

(3)最后一步蒸馏制得晶态碘时,发现冷凝到锥形瓶中的有机物呈淡紫色,推测其原因是__________
Ⅱ.欲配制 480mL0.5mol·L-1 的 NaOH 溶液,试回答下列问题。
(4)配制上述溶液需要的仪器有:药匙、托盘天平、量筒、玻璃棒、________。
(5)某学生实际配制的 NaOH 溶液的浓度为 0.51mol·L-1,原因可能是_________。
A 使用滤纸称量 NaOH 固体 B 容量瓶中原来存有少量水
C 溶解后的烧杯未经多次洗涤 D 用胶头滴管加水定容时俯视刻度
E 加水时超过刻度线,用胶头滴管吸出 F 转移溶液之前未经冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分离提纯的描述不正确的是

A.分离KCl和MnO2混合物的步骤:加水溶解、过滤,滤渣洗涤后干燥,滤液蒸发结晶
B.蒸馏提纯时温度计的位置如图1所示,收集的产品中混有低沸点杂质
C.NaCl晶体中混有少量KNO3杂质的分离方法为:加水溶解、蒸发结晶、趁热过滤、洗涤、干燥
D.萃取溴水时,加入适量CCl4,转移至分液漏斗中,如图2,用力振摇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用如图装置制得氯气并与铝粉反应制备无水AlCl3。已知AlCl3在183°C升华,遇潮湿空气即反应产生大量白雾。请回答问题:
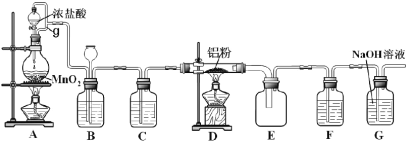
(1)A中反应的化学方程式为_________;HCl在反应中表现出的性质为______(填:酸性、氧化性或还原性)。
(2)A中g管的作用是________。
(3)B中盛放饱和食盐水的作用是________;若D中生成的AlCl3凝华堵塞导管,B中可观察到的现象为________。
(4)C和F所装试剂相同,其中F的作用是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中分子数相同的是( )
A.2 L CO和2 L CO2B.9 g H2O和标准状况下11.2 L CO2
C.标准状况下1 mol O2和22.4 L H2OD.0.2 mol NH3和4.48 L HCl气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A.NaCl(aq) ![]() Na(s)
Na(s) ![]() Na2O2(s)
Na2O2(s)
B.SiO2(s) ![]() Si(s)
Si(s) ![]() SiCl4(l)
SiCl4(l)
C.SO2(g) ![]() NH4HSO3(aq)
NH4HSO3(aq) ![]() (NH4)2SO4(aq)
(NH4)2SO4(aq)
D.Cu2(OH)2CO3(s) ![]() CuO(s)
CuO(s) ![]() Cu(OH)2(s)
Cu(OH)2(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)今有五种物质:①铜线 ②熔化的NaCl ③NaCl晶体 ④氨气 ⑤液态氯化氢,其中能导电的物质是__;属于电解质的是___;属于非电解质的是___。
(2)0.5molH2SO4的质量是__g,能中和___molNaOH,该硫酸所含氢元素的质量与___molNH3中所含氢元素的质量相同。
(3)相同质量的CH4和H2S中分子个数比为___。
(4)在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,n(K+)=0.2mol,n(Mg2+)=0.15mol,n(Cl-)=0.2mol,则n(NO3-)为(_____)
A.0.05mol B.0.20mol C.0.30mol D.0.40mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究CO2的利用对促进低碳社会的构建具有重要的意义。
(1)现有反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。在850℃时,K=1。
CH3OH(g)+H2O(g) ΔH<0。在850℃时,K=1。
①如果上述反应的平衡常数K值变大,该反应___(填字母)。
a.一定向正反应方向移动 b.在平衡移动过程中正反应速率先增大后减小
c.一定向逆反应方向移动 d.在平衡移动过程中逆反应速率先减小后增大
②若反应容器的容积为2.0L,反应时间4.0min,容器内气体的物质的量减小了0.8mol,在这段时间内CO2的平均反应速率为___。
③在850℃时,若向1L的密闭容器中同时充入3.0mol CO2、1.0molH2、1.0molCH3OH、5.0molH2O(g),上述反应向___(填“正反应”或“逆反应”)方向进行。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是___。
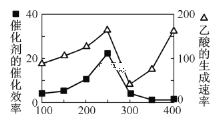
②为了提高该反应中CO2的转化率,可以采取的措施是___。(写一条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com