
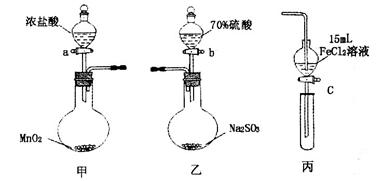
| | 步骤3溶液中含有的离子 | 步骤5溶液中含有的离子 |
| I | 既有Fe3+又有Fe2+ | 有SO42- |
| Ⅱ | 有Fe3+无Fe2+ | 有SO42- |
| Ⅲ | 有Fe3+无Fe2+ | 有Fe2+ |
 MnCl2+2H2O+Cl2↑(2)70%的硫酸中c(H+)比98%的硫酸大
MnCl2+2H2O+Cl2↑(2)70%的硫酸中c(H+)比98%的硫酸大 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。

科目:高中化学 来源:不详 题型:实验题
| | 选用试剂 | 实验现象 |
| 方案1 | | |
| 方案2 | | |
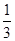 的Br-被氧化成Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
的Br-被氧化成Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
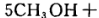
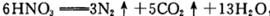 下列说法正确的是
下列说法正确的是| A.CH3OH被氧化,表现氧化性 |
| B.此条件下还原性强弱为:N2>CH3OH |
| C.若氧化产物比还原产物多0.2 mol,则该反应中转移3 mole- |
| D.该反应过程中断裂的化学键既有极性键又有非极性键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水层显棕黄色 | B.水层无色 | C.四氯化碳层显红棕色 | D.四氯化碳层无色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 | 现象:溶液变成黄色。 结论: 。 |
| 步骤2:__________________________ __________________________________ | 现象: ; 结论: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
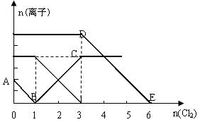
| A.还原性I->Fe2->Br- |
| B.原混合溶液中c(FeBr2) = 4mol/L |
| C.当通入Cl2 2mol时,溶液中已发生的离子反应可表示为:2Fe2+ + 2I- + 2Cl2 → 2Fe3+ + I2 + 4 Cl- |
| D.原溶液中n(Fe2+) :n(I-) :n(Br-) =" 2" :1 :3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O| A.反应(1)和(2)均为氧化还原反应 |
| B.反应(1)的氧化剂是O2,还原剂是FeO?Cr2O3 |
| C.高温下,O2的氧化性强于Fe2O3,弱于Na2CrO4 |
| D.反应(1)中每生成1molNa2CrO4时电子转移3mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.①④⑤⑥⑦ | C.②③④ | D.①③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com