
【题目】实验室可通过蒸馏石油得到多种沸点范围不同的馏分,装置如图所示。下列说法不正确的是
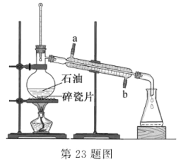
A.沸点较低的汽油比沸点较高的柴油先馏出
B.蒸馏烧瓶中放人沸石可防止蒸馏时发生暴沸
C.冷凝管中的冷凝水应该从 a 口进 b 口出
D.温度计水银球的上限和蒸馏烧瓶支管口下沿相平
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
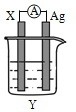
(1)电极X的材料是______;电解质溶液Y是AgNO3,则在银电极上析出______单质;
(2)银电极为电池的______极,发生的电极反应为______;X电极上发生的电极反应为______;
(3)外电路中的电子是从______电极流向______电极(从铜、银中选填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)![]() PCl5(g)。达平衡时,PCl5为0.40 mol,如果此时移走1.0 mol PCl3和0.50 mol Cl2,在相同温度下再达平衡时,下列说法不正确的是
PCl5(g)。达平衡时,PCl5为0.40 mol,如果此时移走1.0 mol PCl3和0.50 mol Cl2,在相同温度下再达平衡时,下列说法不正确的是
A. PCl5的物质的量大于0.20 molB. PCl5的质量分数减少
C. 平衡常数不变D. 混合气体的黄绿色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。①A元素最外层电子数是次外层电子数的2倍。②B的阴离子和C的阳离子与氖原子的电子层结构相同。③在通常状况下,B的单质是气体,0.1 mol B的气体与足量的氢气完全反应共有0.4 mol电子转移。④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应可生成B的单质。⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请回答下列问题:
(1)写出A元素的最高价氧化物的电子式_____________。
(2)B元素在周期表中的位置为_____________。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有______________。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为______________。
(5)C与D能形成2∶1的化合物,用电子式表示该化合物的形成过程______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与H2完全加成后,不可能生成2,2,3-三甲基戊烷的烃是( )
A. 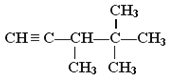 B.
B. 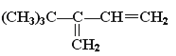
C. CH2=CHC(CH3)2CH(CH3)2D. (CH3)3CC(CH3)=CHCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰电池的反应方程式为 2MnO2+Zn+2H2O===2MnOOH+Zn(OH)2,其构造如图所示。有关说法不正确的是( )

A.负极反应式:Zn+2OH--2e-===Zn(OH)2
B.放电时正极MnO2得到电子,发生氧化反应
C.该电池使用一段时间后,电解液pH增大
D.放电时,锌粉失去的电子,从负极通过外电路流向正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种化合物,有的是药物,有的是香料。它们的结构简式如下所示:
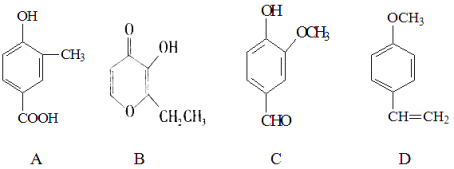
(1)化合物A的分子式是 ;A中含有的官能团的名称是 、
(2)A、B、C、D四种化合物中互为同分异构体的是(填序号) ;
(3)化合物B的核磁共振氢谱中出现 组峰;
(4)1mol D最多能与 mol的氢气发生加成反应;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有某硫酸和硝酸的混合溶液20mL,其中含有硫酸的浓度为2mol/L,含硝酸的浓度为1mol/L,现向其中加入0.96g铜粉,充分反应后(假设只生成NO气体),最多可收集到标况下的气体的体积为
A.89.6mLB.112mLC.168mLD.224mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尿素是最简单的有机化合物之一,是哺乳动物和某些鱼类体内蛋白质代谢分解的主要含氮终产物。
(1)尿素[(NH2)2CO]是含氮量最高的固体氮肥,其理论含氮量为________%(保留 1 位小数),尿素中 N 的化合价为________.
(2)二氧化碳、氨在高温、高压下合成氨基甲酸铵,氨基甲酸铵再发生分解反应可得到尿素。写出该分解反应的化学方程式:____________________________。
(3)可用酸性(NH2)2CO 水溶液吸收氮氧化物 NOx。吸收过程中存在 HNO2 与(NH2)2CO 生成 N2 和CO2 的反应,写出该反应的化学方程式_______________________________ 当生成 1 mol N2 时,转移的电子数为 __________ .
(4)也可用水吸收氮氧化物 NOx,已知 NO2 溶于水的相关热化学方程式如下:
2NO2(g)+H2O(l)![]() HNO3(aq)+HNO2(aq) △H=116.1 kJ·mol1
HNO3(aq)+HNO2(aq) △H=116.1 kJ·mol1
3NO2(g)+H2O(l)![]() 2HNO3(aq)+NO(g) △H=136.2kJ·mol1。
2HNO3(aq)+NO(g) △H=136.2kJ·mol1。
则用稀硝酸吸收NO的反应HNO3(aq)+2NO(g)+H2O(l)=3HNO2(aq)△H=___kJ·mol1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com