
| A. | 丁烷的结构简式为CH3CH2CH2CH3 | B. | 一氯乙烷的结构式为CH3Cl | ||
| C. | 四氯化碳的电子式为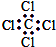 | D. | 苯的分子式为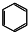 |
分析 A.丁烷为含有4个碳原子的烷烃,不存在支链;
B.结构式中需要用短线代替所有的共用电子对,且CH3Cl为一氯甲烷的结构简式;
C.没有写氯原子的3对孤电子对;
D. 为结构简式,不是分子式.
为结构简式,不是分子式.
解答 解:A.丁烷为含有4个碳原子的直链烷烃,其结构简式为:CH3CH2CH2CH3,故A正确;
B.CH3Cl一氯甲烷的结构简式,一氯乙烷正确的结构式为: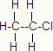 ,故B错误;
,故B错误;
C.四氯化碳中氯原子最外层达到8电子稳定结构,四氯化碳正确的电子式为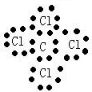 ,故C错误;
,故C错误;
D.苯的分子式为C6H6, 为结构简式,故D错误;
为结构简式,故D错误;
故选A.
点评 本题考查常见化学用语的表示方法,题目难度中等,涉及结构式、分子式、电子式、结构简式的书写,明确常见化学用语的书写原则为解答关键,试题侧重考查学生的辨别能力.


科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,71g Cl2中所含分子数为NA | |
| B. | 0.1mol/L的H2SO3溶液中,c(H+):c(SO32-)>2:1 | |
| C. | 2L 0.6mol/L的Fe2(SO4)3溶液中,含Fe3+离子总数为2.4NA | |
| D. | 1molNa与足量的O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某些金属的单质和化合物在火焰上灼烧时都能显现特殊的颜色,因此焰色反应是元素的性质 | |
| B. | 钾的焰色为紫色,必须通过蓝色钴玻璃才能观察到 | |
| C. | 焰色反应是物理过程,但也可能伴随着化学变化 | |
| D. | 烟花能显现出五颜六色,与烟花中含有某些金属元素的盐类有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Cl-、H+、SO42- | B. | H+、NO3-、Ba2+、Cl- | ||
| C. | K+、Cl-、H+、SO42- | D. | Ca2+、Na+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为SiH4+3H2O=4H2+H2SiO3,整个系统还必须与氧隔绝,其原因是SiH4+O2=SiO2+2H2O(用化学方程式表示)
(1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为SiH4+3H2O=4H2+H2SiO3,整个系统还必须与氧隔绝,其原因是SiH4+O2=SiO2+2H2O(用化学方程式表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.01×1023个铁原子 | B. | 标准状况下33.6L SO2 | ||
| C. | 1L 1mol/L Na2SO4溶液中的Na+ | D. | 16g氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com